Quality control in ER ・糖鎖合成
30 likes | 136 Vues
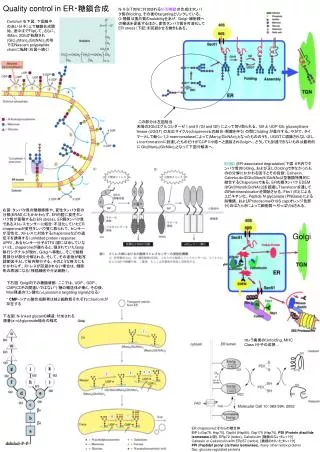
N-X-S/T の N に付加される N- 型糖鎖 の合成はタンパク質の folding, その後の targeting とリンクしている。 O- 糖鎖は蛋白質の solubility をあげ, Golgi ・細胞膜への輸送を促進するほか、変性タンパク質を可溶化して ER stress (下記)を回避させる働きもある。.

Quality control in ER ・糖鎖合成
E N D
Presentation Transcript
N-X-S/TのNに付加されるN-型糖鎖の合成はタンパク質のfolding, その後のtargetingとリンクしている。 O-糖鎖は蛋白質のsolubilityをあげ,Golgi・細胞膜への輸送を促進するほか、変性タンパク質を可溶化してER stress(下記)を回避させる働きもある。 Dolichol(右下図,下図膜中の赤い分子)上で糖鎖合成開始、途中④でFlipして、さらに、4Man, 3Glcが転移され (Glc)3(Man)9(GlcNAc)2の形で⑥Nascent polypeptide chainに転移(右図へ続く) Quality control in ER・糖鎖合成 この部分は左図相当 末端の3Glcはグルコシダーゼ I and II (GI and GII) によって切り取られる。 GII と UDP-Glc glucosyltrans-ferase (UGGT) の反応サイクル(chaperoneとの結合・解離を伴う) の間にfolding が進行する。やがて、タイマーとして働くa-1,2-mannnosidaseによって(Man)8(GlcNAc)2となったもののうち、UGGTに認識されない正しいconformationに到達したものだけがCOP II小胞へと選抜されGolgiへ。どうしても到達できないものは最終的に Glc(Man)8(GlcNAc)2となって下図分解系へ。 ERAD (ER-associated degradation)下図:ER内でタンパク質のfolding、および正しくfoldingできなかったものの分解にかかわる因子とその役割: Calnexin, CalreticulinはGlc(Man)9(GlcNAc)2型糖鎖特異的に結合するChaperoneである。ERの膜タンパク EDEMはGlc(Man)8(GlcNAc)2を認識しTransloconを通してのRetrotranslocationを開始させる。Fbs1 (E3)によるユビキチン化、Peptide N-glycanase (PNGase)による脱糖鎖、およびProteosomeの19S cap(オレンジ色部分)のはたらきによって細胞質へ引っぱり出される。 右図:タンパク質の糖鎖修飾や、変性タンパク質の分解(ERAD)にもかかわらず、ER内腔に変性タンパク質が蓄積すると(ER stress)、ER膜タンパク質であるストレスセンサーに結合・不活化していたER chaperoneが変性タンパク質に取られて、センサーが活性化、ストレスに対処するchaperoneなどの遺伝子を誘導する(unfolded protein response: UPR)。あるセンサー分子ATF6(図には示していない)は、chaperoneが離れると、隠されていたGolgi移行シグナルが現れ、Golgiへ移動し、そこで細胞質部分が部分分解される。そして、その産物が転写調節因子として核内移行する。そのような努力にもかかわらず、ストレスが回避されない場合は、細胞死の原因になる(神経細胞や分泌細胞)。 Golgi or Derlin channel 下右図:Golgi内での糖鎖修飾 ここでは、UDP-, GDP-, CMP(CDPの間違いではない*)-糖の輸送体が働く。その後、Man残基のリン酸化(=Lysosome targeting signalとなる) * CMP–シアル酸合成酵素は核と細胞質それぞれにIsoformが存在する 下左図:N-linked glycanの構造:付加される順番(a-n)とglycoside結合の様式 コレラ毒素のUnfolding, MHC Class I分子の成熟… Molecular Cell 10: 983-994, 2002 ER chaperoneとそれらの複合体 BiP (=Grp78, Hsp70), Grp94 (Hsp90), Grp170 (Hsp70), PDI (Protein disulfide isomerase上図), ERp72 (redox), Calreticulin [糖鎖のないタンパク] Calnexin or Calreticulin with ERp57 (redox), [糖鎖の付いたタンパク] PPI (Peptidyl prolyl cis/trans isomerase), many other redox proteins Grp: glucose regulated proteins