MATERIA
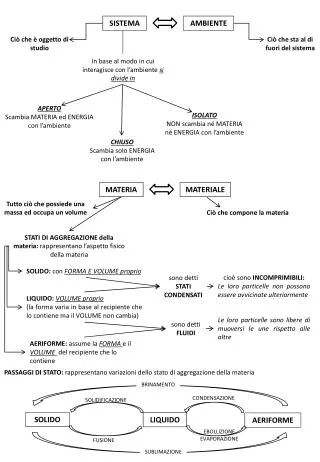
MATERIA. Lic. Amalia Vilca Pérez. ¿Qué es materia?. Todo aquello que ocupa un lugar en el espacio, tiene masa y requiere energía para un cambio o transformación. PROPIEDADES. Propiedades fundamentales Forma: Depende de su naturaleza o fenómenos externos. Volumen: Sus dimensiones.

MATERIA
E N D
Presentation Transcript
MATERIA Lic. Amalia Vilca Pérez
¿Qué es materia? • Todo aquello que ocupa un lugar en el espacio, tiene masa y requiere energía para un cambio o transformación
PROPIEDADES Propiedades fundamentales Forma: Depende de su naturaleza o fenómenos externos. Volumen: Sus dimensiones. Tipos de propiedades: Físicas * Extensivas. * Intensivas. Químicas: Todas las reacciones Ejp: combinación, reacción, oxidación, sabor, olor, reducción, combustión, etc.
Propiedades FÍSICAS de la materia Extensivas: se relacionan con la estructura química externa; es decir, aquellas que podemos medir y que dependen de la cantidad y forma de la materia. Ejemplo: peso, volumen, longitud, energía potencial, calor, etcétera. Intensivas:se relacionan con la estructura química interna de la materia. Ejemplo:temperatura, punto de fusión, punto de ebullición, calor específico o concentración (ver glosario para estos tres últimos términos), índice de refracción, entre otros aspectos.
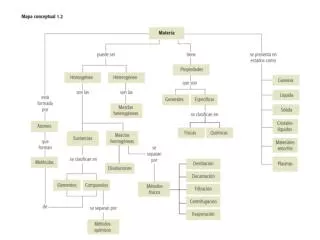
PROPIEDADES DE LA MATERIA Es el conjunto de características que las identifican y les proporcionan una inconfundible identidad, dichas características se llaman propiedades.
Clasificación de las propiedades • PROPIEDADES FISICAS: Son aquellas que pueden ser determinadas sin que ocurra ningún cambio en la composición del material
PROPIEDADES ESPECÍFICAS o INTENSIVAS viscosidad conductividad textura brillo color maleabilidad Temperatura de fusión y ebullición
PROPIEDADES ESPECIFICAS CONTINUACIÓN…. ductibilidad textura dureza solubilidad densidad color Sabor
1.-PROPIEDADES GENERALES O EXTENSIVAS masa inercia volumen divisibilidad longitud
PROPIEDADES QUIMICAS • Combustión, • Digestión, • Corrosión, • combinación, • reacción, • oxidación, • reducción.
Transformaciones de la Materia • Fenómeno: Cambio que experimenta la materia. • Fenómeno Químico: Cambio químico siempre altera composición de la materia. - sucesos observables. -Pueden ser medidos. Ejemplos: • las reacciones de oxidación • las reacciones de combustión • la formación de una sal • el fraguado del cemento
Fenómenos Físicos y Químicos • Fenómeno Físico: Cambios físicos sin que se produzca alteración en la composición de la materia. Ejp: • la elasticidad de una barra de metal • la fuerza ejercida por un cuerpo sobre otro • una pelota rodando • el agua hirviendo
FENOMENOS Cambios o modificaciones que experimentan las sustancias bajo la acción de las diferentes formas de energía
Cambios o fenómenos físicos Ejemplos: Reflexión y refracción de la luz *Arcoiris • Fusión de la cera • Disolución del azúcar • Electrización del vidrio • Dilatación de un metal • Movimiento de las capas • Transmisión de calor • Cambios de estado. No alteran la composición intima de las sustancias o solo hacen por un momento aparente o transitorio (reversibles)
FENOMENOS QUÍMICOS • Corrosión de los metales • Explosión de una bomba Acumulador • Fenómenos de visión • Revelado de una foto • Encender un cerillo • Fenómeno de Fotosíntesis Cambio experimentado donde se modifica permanentemente la naturaleza íntima de las sustancias y no es reversible. Ejemplos: • Digestión de los alimentos Acción de los medicamentos
Destilación Procedimiento: para la separación y purificación de líquidos, y es el que se utiliza siempre que se pretende separar un líquido de sus impurezas no volátiles.
Evaporación Ejp: Las Salinas. Del agua de mar se obtiene sales: cloruro de sódio, de potasio, etc…
Evaporación: Es la operación por la cual se separa un sólido disuelto en un liquido por incremento de temperatura hasta que él liquido hierve, el sólido queda en el recipiente y él liquido se evapora.
Centrifugación Procedimiento que acelera la sedimentación. Mediante un movimiento de rotación constante y rápido, lográndo que las partículas de mayor densidad, se vayan al fondo y las más livianas queden en la parte superior
Centrifugación: Método utilizado para separar un sólido de un liquido mediante un aparato llamado centrifuga, por el cual un movimiento de translación acelerado aumenta la fuerza gravitacional provocando un sedimento del sólido o partículas de mayor densidad. Filtración: Separación de un liquido utilizado un medio poroso llamado filtro.
Filtración • Paso de la mezcla por medio de papeles filtros de distintos tamaños. • Método sencillo y barato. • No altera las propiedades de las sustancias
Cristalización • Método para separar una mezcla de sólidos que sean solubles en el mismo disolvente. Decantación • Se aplica para mezclas sólido insoluble – líquido.
Métodos de separación de mezclas DESTILACIÓN Decantación: Método utilizado para la separación de un sólido de grano grueso e insoluble, de un liquido por la separación de 2 líquidos no miscibles de diferente densidad. Método que permite separar mezclas de líquidos miscibles aprovechando sus diferentes puntos de ebullición.
Magnetismo Se vale de las propiedades magnéticas de algunos materiales. Se emplea para separar mezclas en donde uno de sus componentes es magnético.
Tamizado Se aplica para mezclas de sólidos con diferentes tamaños de partícula, utilizando para ello mallas.
Sublimación Es la separación de componentes de la mezcla heterogénea, donde sus componentes son sólidos y uno de ellos se evapora por aumento de la temperatura.
Adsorción: Es la capacidad que tienen algunas sustancias de retener sobre la superficie algunas partículas que dan olor, sabor, color o una apariencia turbia. Cromatografía: este método consiste en separar mezclas de gases o líquidos por el paso de estos por un medio poroso y adecuarlo con la ayuda de solventes.
Los electrones giran alrededor del núcleo en regiones del espacio denominadas orbitas
En el átomo distinguimos dos partes: • LA CORTEZA • Es la parte exterior del átomo. En ella se encuentra los electrones, con carga negativa. Estos , ordenados en distintos niveles , giran alrededor del núcleo. • La masa de un electrón es unas 2000 veces menor que la de un protón. • EL NÚCLEO • Es la parte central del átomo y contiene partículas con carga positiva, los protones, y partículas que no poseen carga eléctrica, es decir son neutras, los neutrones. • La masa de un protón es aproximadamente igual a la de un neutrón.
Todos los átomos de un elemento químico tienen en el núcleo el mismo número de protones. Este número, que caracteriza a cada elemento, es el número atómico, y se representa con la letra Z.
DE ACUERDO A LA INFORMACION ANTERIOR DIGA DE QUE ELEMENTO SE TRATA En la tabla periódica encontramos esta información para cada elemento Los elementos se ubican en orden creciente de su número atómico en la tabla periódica.