Масс спектрометрия
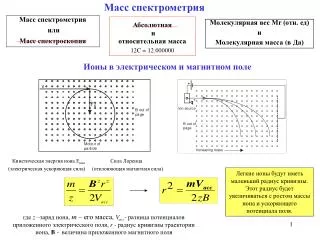
Масс спектрометрия. Масс спектрометрия или Масс спектроскопия. Абсолютная и относительная масса 12C = 12.000000. Молекулярная вес М r (отн. ед) и Молекулярная масса ( в Да). Ионы в электрическом и магнитном поле.

Масс спектрометрия
E N D
Presentation Transcript
Масс спектрометрия Масс спектрометрия или Масс спектроскопия Абсолютная и относительная масса 12C = 12.000000 Молекулярная вес Мr (отн. ед) и Молекулярная масса (в Да) Ионы в электрическом и магнитном поле Кинетическая энергия иона Екин Сила Лоренца (электрическая ускоряющая сила) (отклоняющая магнитная сила) Легкие ионы будут иметь маленький радиус кривизны.Этот радиус будет увеличиваться с ростом массы иона и ускоряющего потенциала поля. гдеz–заряд иона, m– его масса, Vacc-разница потенциалов приложенного электрического поля, r- радиус кривизнытраектории иона, B- величина приложенного магнитного поля
От ионов в растворе - к ионам в газовой фазе Перенос ионов из раствора в газовую фазу требует большой энергии и не происходит самопроизвольно. Например, перенос иона Na+ требует 98 ккал/моль. Поэтому перенос десятков тысяч ионoв в газовую фазу из раствора в масс спектрометре требует очень большой затраты энергии • Способы получения ионов • Удаление электронов из молекулыдля получения позитивно заряженного катиона, который может быть ускорен либо увеличением отрицательного градиента или уменьшением позитивного градиента поля. • Добавление электрона к молекуле для получения отрицательно заряженного аниона. В этом случае знак ускоряющего напряжения противоположен знаку, требуемому для катиона. • 3) Удалением или добавления протона. В этом случае результирующая масса будет отличаться на ±1 от массы исходного нейтрального иона. Техника ионизации Электронная ионизация Ионизация полем Бомбардировка быстрыми атомами Плазменная ионизация Лазерная ионизация с использованием матрицы (MALDI) Ионизацияэлектрораспылением (ESI)
Лазерная ионизация с использованием матрицы (MALDI) Специфика лазерного излучения. Два типа лазеров используются в технике MALDI: Инфракрасный лазер, возбуждающий вибрационные моды и УФ - лазер, возбуждающий электронные переходы в молекуле. Длина импульса обычно составляет 100 нсили меньше. Большие длины импульсов обычно приводят к тепловому разложению образца. Матрица – ключевой элемент техники. Ее главная роль: содержать хромофор, поглощающий лазерное излучение. Последнее не должно затрагивать хромофоры исследуемой молекулы.Матрица испаряясь переходит в газовую фазу, увлекая за собой исследуемую молекулу. Специфика масс- спектрометра Поскольку большинство лазерных источников являются пульсирующими, то для регистрациииспользуются такие методы как метод времени пролета или метода ионного циклотронного резонанса. Точность определения массы составляет ±0.01% (±1 Da при молекулярной массе 10 кДa).
Ионизация электрораспылением Схематическое представление прохождения ионов от кончика иглы, содержащего раствор биологических макромолекул, до детектора масс спектрометра. Раствор белка (объем - 1-2 μл, концентрация - 5 μM)выходит из тонкого капилляра (внутренний диаметр около 10 μм). К концу капилляра, покрытого золотом, прикладывается высокое напряжение (обычно несколько кВ), вызывая распад капель на очень мелкие капли. Десольватация последних приводит к появлению облака молекул, которые детектируются масс спектрометром. Точность определения молекулярных масс составляет 0.001-0.005%.
Инструменты и техника регистрации в масс спектрометрии Single and double focusing mass spectrometers Fourier transform mass spectrometry Quadrupole mass filter Triple mass filter Quadrupole ion trap Ion cyclotron resonance mass spectrometry
Определение масс белков Моноизотопная масса +1Da horse cytochromec +2Da +3Da horse myoglobin [Arg8]-вазопресин 1084.446 МАЛДИ спектр высокого разрешениябелка [Arg8]-вазопресина. Основной спектр1084.446 относится к «моноизотопному» пику протонированного белка. Три пика более высокой массы относятся к вкраплению в белок изотопа 13C, доля встречаемости которого в природе равна 1.108%. ESI-FTIR масс спектр двух белков: цитохрома c и миоглобиналошади. Концентрация образца 0.4 нM. Общее количество белка около 135 зM(~ 80 000 молекул). 1 зепто моль = 10-21 моля
Молекулярная масса нейтральной молекулы M может быть найдена из значений регистрируемых масс m1 и m2 и (что эквивалентно значениям m/z) и числа добавленных зарядов или протонов n1 иn2: М= n2 (m2 - 1) (A) где n1 = n2+1 и n2= (m1-1)/(m2-m1) Следовательно, M, можно рассчитать, если брать пики регистрируемых масс попарно. Цитохром с Применяя формулу (А) для расчета молекулярной массы цитохрома c с использованием двух соседних пиков с = 952.3 и = 1031.3, получим для следующее значение: Это означает, что 12 положительных зарядов ассоциированы с относительной массой, равной 1031.3. Молекулярная масса в этом случае рассчитывается как М = n2 (m2 -1) и равна 12363.6. Рассматривая следующие два пика с относительными массами = 884.3 и = 952.3, мы получим: или Z = 13, т.е. 13 положительных зарядов ассоциированы с относительной массой 952.3. Рассчитанная из этих пиков молекулярная масса равна 12366.9.
Сворачивание белков: конечные и промежуточные состояния Различные моменты времени Различные pH Цитохром c АпомиоглоинКислая денатурация миоглобина
Нуклеиновые кислоты и их комплексы с белками. Проблема: «любовь НК» к ионам. 5 мМ Мg bacterial plasmid (pBR322) Мономер Димер 1 mM Mg Гистограмма средних массобразца ДНК. Доминантный пик 2.88 MДa соответствует Na-бактериальной ДНК плазмиде (pBR322), а меньший пик ее димеру(Benner, 1997). Расчетное значение молекулярной массы 30S субьединицы равно 852187 ± 3918 Дa. Этавеличина на 0.6% отличается от «точного значения», вычисленного из составляющих ее компонентов (16S РНК и белков).
Статический и динамический протеомы и масс-спектрометрия Две стратегии анализа протеома методом масс спектрометрии (Godovach-Zimmermann and Brown, 2001).
Формирование изображения с помощью масс спектрометрии Методология пространственного анализа ткани методом MALDI-MS. Замороженные секции помещаются на металлической плате и покрываются UV- абсорбирующей матрицей. Затем они помещаются в масс-спектрометр и сканируются лазерным лучом. (Stoeckli et al., 2001, Nature Medcine, 7, p.494). Масс спектрометрическое изображение замороженных секций ткани мозга мыши. (а) Оптическое изображение замороженной секции на золотой подложке. (b) Распределение белков с m/z =8528 в области центральной коры головного мозга (c) Тоже дляm/z 6716 в области медиальных сучковатых ядер. (d)Тоже дляm/z2564 в области среднего мозга.