Les PPARs
Matthieu Ruas Laurent Sattler Nicolas Stahl Nicolas Urbaniak François Wernette. Tutrice : Mme Matz-Westphal. Les PPARs. Peroxisome-Proliferator-Activated-Receptor. Plan de l’exposé. I. Mécanisme d’action général PPAR a et sa classe thérapeutique Fibrates

Les PPARs
E N D
Presentation Transcript
Matthieu Ruas Laurent Sattler Nicolas Stahl Nicolas Urbaniak François Wernette Tutrice : Mme Matz-Westphal Les PPARs Peroxisome-Proliferator-Activated-Receptor
Plan de l’exposé • I. Mécanisme d’action général • PPARa et sa classe thérapeutique • Fibrates • PPARg et sa classe thérapeutique • Thiazolidinediones • IV. Horizons thérapeutiques • PPARb/d • Co-agonistes et PPARpan • V. Conclusion www.hindawi.com
I. Mécanisme d’action • Les PPARs ( Peroxysomes Proliferator Activated Receptors) : • Appartiennent à la famille des récepteurs nucléaires • Facteurs de transcription activés par des ligands endogènes et synthétiques PPARs PPARg PPARa PPARb/d Organes du métabolisme des AG Muscle squelettique et cardiaque Tissu adipeux
Mécanisme d’action général Ligands endogènes et médicaments Eicosanoïdes Prostaglandines Leukotriènes Acides Gras PPAR Membrane nucléaire RXR Changement conformationnel Ejection des co-répresseurs Recrutement des co-activateurs Co-répresseurs Activation de la transcription ADN Pol II ADN Pol II PPRE PPRE
II. Les PPARα Implications en thérapeutique : Les Fibrates
Expression tissulaire de PPARα MUSCLE SQUELETTIQUE REIN COEUR PPAR α INTESTIN FOIE = organes produisant un fort catabolisme des AG + dans les monocytes / macrophages, cellules endothéliales, lymphocytes T, cellules dendritiques…
Intérêt thérapeutique FIBRATES • Agonistes sélectifs des PPAR α • Indications: • hypertriglycéridémie • hypercholestérolémie
VLDL HDL ↑ Apo A-V ↓ Apo C-III ↑ LPL (cœur + muscle) Chylomicrons Mécanisme d’action des FIBRATES régulation de l’expression des gènes PPAR α fibrates Hépatocyte Vaisseau sanguin ↑ ↑Apo A-I, Apo A-II ↑ transport reverse du cholestérol ↓ triglycérides action hypotriglycéridémiante action hypocholestérolémiante
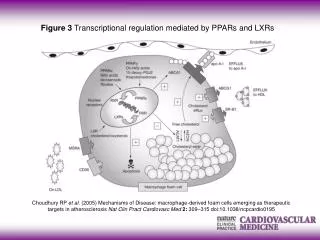
PPAR α et athérosclérose Cause majeure de mortalité de maladies cardiovasculaires dans les pays développés Mécanismes de l’athérogénèse Paroi vasculaire • lésion vasculaire de l’intima • accumulation de LDL dans le • sous-endothélium • modification oxydative des LDL • phénomène inflammatoire: • recrutement des monocytes • macrophages en c spumeuses • accumulation de lipides extra CR • migration et accumulation de CML vasculaires • formation d’une matrice extra C • = constitution de la chape fibreuse endothélium LDL thrombus Lumière vasculaire plaque fibrolipidique= plaque d’athérome mature Monocyte Macrophage cœur lipidique de la plaque = centre athéromateux
PPAR α et athérosclérose • Complications: • Sténose artérielle (↓ diamètre vasculaire) • Perte du pouvoir anti-thrombotique de l’endothélium (lésions) • Rupture plaque: sang en contact avec le sous-endothélium ischémie thrombose embolie • Risque lié au thrombus formé: • pulmonaire • cardiaque: IDM • cérébrale: AVC
PPAR α et athérosclérose • Principaux facteurs de risque: • Dyslipidémies • Phénomènes inflammatoires • Hypertension Action de PPAR α: prévient et limite l’évolution de la plaque d’athérome
LDL lumière vasculaire PPAR α et athérosclérose • Actions de PPAR α : dans les dyslipidémies (vu précédemment cf. fibrates) • action hypotriglycéridémiante: ↓ TG dans les VLDL ↓ TG dans les LDL circulantes LDL : ↑ taille, ↓ densité Limite l’accumulation de LDL dans le sous-endothélium
↓l’expression de molécules d’adhésion endothéliales ↓ la perméabilité vasculaire (monocytes) ↓ la perméabilité vasculaire (monocytes) PPAR α et athérosclérose 2) Actions de PPAR α : dans les phénomènes inflammatoires • Aux cellules du système immunitaire: Lymphocytes T • ↓ production de cytokines pro-inflammatoires (TNFα, IFNγ , IL-2) • Aux cellules endothéliales: • ↑ l’expression de la NO synthase: ↓ l’expression de VCAM-1
Effet anti-hypertenseur : ↓ le risque de lésions de l’intima Limite l’évolution de la plaque d’athérome PPAR α et athérosclérose 3) Actions de PPAR α : dans l’hypertension • ↓ production d’endothéline-1 (ET-1) • ↑ expression de la NO synthase : ↑production NO Vasodilatation De plus: • ↓ production d’ET-1 ↓ prolifération des CML vasculaires
Effet anti-thrombogène PPAR α et athérosclérose 4) Actions de PPAR α : dans la stabilisation de la plaque d’athérome • inhibe l’expression de l’enzyme MMP9 (métalloprotéase de la matrice) par le macrophage • limite la production de cytokines pro inflammatoires par le macrophage, responsables de l’activation de la sécrétion de MMPs et de l’inhibition de la synthèse de collagène limite la dégradation de la matrice extracellulaire • Préservation de la chape fibreuse • Maintien d’une barrière sang / sous-endothélium
III. Les PPARγ Implications en thérapeutique : Les Thiazolidinediones
Isoformes & Localisation Il existe 3 isoformes de PPARγ ayant des localisations différentes dans l’organisme : • γ1 : Ubiquitaire (gros instestin, cellules hématopoïétiques, tissu adipeux) • γ2 : Présent dans le tissu adipeux (pré-adipocytes) • γ3 : Majoritairement présent dans les macrophages et dans le gros intestin
Thérapeutique : les TZD Les TZD (Thiazolidinedione) sont des agonistes des PPARγ ayant pour objectif thérapeutique : • le traitement du diabète de type II (non insulino requérant). En mono, bi, ou tri thérapie (sulfamides anti-diabétiques, metformine). Action : Augmentation de la sensibilité à l’insuline (Muscle, Foie, Tissu adipeux). Autres effets : • Protection des cellules β du pancréas.
Un peu d’Histoire… Le premier agoniste PPARγ de la classe des TZD a été découvert en 1995. Il s’agit de la Troglitazone(Rezulin®), depuis retiré du marché : 2ème génération : • Pioglitazone (Actos® 1999) • Rosiglitazone (Avandia® 1999) 3ème génération : RS5444, 50 fois plus puissant que Rosiglitazone
Effets glucidiques… • Au niveau du tissu adipeux : • Augmentation de production d’adiponectine => Augmentation d’entrée de glucose dans les tissus (Activation GLUT4). • Sensibilisation à l’insuline par la baisse du TNFα (↓ activité IKKβ) • On observe au niveau hépatique et musculaire : • Une baisse de la néoglucogenèse • Une baisse de la β-oxydation => Utilisation préférentielle du glucose par les tissus
…et effets lipidiques. Au niveau du tissu adipeux : • Différentiation des pré-adipocytes en adipocytes • ↓ de l’expression des enzymes de la β-oxydation • ↑ du stockage des acides gras (ScavengerReceptors : CD36) De plus : • ↓ des triglycérides plasmatiques (↑ LPL & ↓ ApoC-III) => augmentation de l’apport d’acides gras au niveau du tissu adipeux et des tissus. => Stockage d’acides gras : Prise de poids.
Objectif : • Quelles solutions ? • PPARβ/δ ? • des co-agonistes ?
IV. Horizons thérapeutiques 1) Les PPAR β/δ Ils sont ubiquitaires mais majoritairement exprimés dans le muscle squelettique et cardiaque
Les PPARb/d Effets de leur activation • Utilisation privilégiée des AG au glucose pour la production d’énergie dans le muscle et dans le cœur Prévention de l’hypertrophie et de l’insuffisance cardiaque congestive • Améliore la captation du glucose dans les muscles squelettiques • Diminue la libération du glucose par le foie • Augmente la glycolyse et l’utilisation du glucose par la voie des pentoses phosphates Amélioration de la tolérance au glucose et de la sensibilité à l’insuline
Les PPARb/d Effets de leur activation www.3dchem.com • Inhibition de l’expression des gènes pro-inflammatoires dans les macrophages et réduction de la formation de plaques d’athérosclérose. • Effet sur les fibres musculaires (cf schéma)
Effets sur les fibres musculaires Fibres IIb : glycolyticfasttwitch Glucose Production d’ATP Ago PPARb/d Fibres: I oxydative slowtwitch IIa : mixed oxydative/glycolytic Fibres IIb : glycolyticfasttwitch Acides gras Production d’ATP
Les PPARb/d Effets de leur activation • Augmente la capture des AG par le muscle squelettique • Augmente l’expression des gènes impliqués dans l’hydrolyse des triglycérides (HSL), et de l’oxydation des AG dans les adipocytes (CPT1) • Effets sur les fibres musculaires Contrôle de la prise de poids
IV. Horizons thérapeutiques 2) PPARγ et développements récents
1) Les co-agonistes Intérêt principal : limiter les effets secondaires inhérents à l’activation des PPAR γ A) Co-agonistesγ/α • Classe des GLITAZARS : • Muraglitazar (BMS) : abandonné en phase II (TIA, CHF)
Tesaglitazar : Stoppé en phase III (DFG ↓) • Ragaglitazar : stoppé en phase II • TAK-559 et KRP-297 : en cours de développement • Ratios γ/α différents
Ago γ/α Effet « TZD like» Effet « Fibrates like» Effets glucidiques = thérapeutiques Effets lipidiques = indésirables ↑β-oxydation : ↓ AG ↑LPL : ↓TG ↓ Cholestérol Sensibilisation Insuline ↑différenciation adipocytaire ↓ β-oxydation Etc… PPAR γ PPAR α Effets lipidiques Prise de poids Diminution
B) Co-agonistes γ / β(δ) • Même principe que co-agonistes γ/α • Essais pré-cliniques: Merck: « Compound 23 » • Lilly : « Compound 20 » • Aucune AMM pour le moment • Ratios γ / β(δ) plus difficiles a déterminer
2) Les PPARpan • Pan Agonistes = agonistes triples : α / β(δ) / γ PPARpan PPAR β(δ) PPAR α Synergie d’action PPAR γ Effet anti-inflammatoire ↓ cytokines pro-infla Effets glucidiques ↑ sensibilité Insuline Effets lipidiques ↓ prise de poids Contrôle lipémie
GW 677954 (GSK) - phase II - Hyperglycémie, insulino-résistance, dyslipédémie associée avec T2DM - aucun gain de poids !!! LY 465608 - phase II - mêmes indications - aucun gain de poids !!!
3) Les SPPARMs • Selective PPAR Modulators • Un seul isoforme cible : PPARγ • Dissociation de l’effet glucidique et lipidique par agonisme partielet recrutement différentiel de co-activateurs et de co-répresseurs.
Ago PPAR γ : TZD SPPARM Fixation sur LBD (interaction forte) Ejection des co-répresseurs Changement conformationnel Recrutement de co-activateurs (CBP/p300 ; SRC-1, PBP/DRIP/TRAP220) Action sur ADN Pol II : transcription Fixation sur LBD (interaction faible) Ejection des co-répresseurs Changement conformationnel Recrutement de co-activateurs : Autres co-activateurs Action sur ADN Pol II : transcription modulée Effets glucidiques majoritaires ↑ sensibilité à l’insuline Effets lipidiques prise de poids Effets glucidiques ↑ sensibilité Insuline
SPPARMs - suite Fmoc-L-Leucine GW 0072 AMG 131- recrute moins DRIP 205 (co-activateur de l’adipogénèse) - recrute NcoR (co-represseur lipidique) - phase II - ↓ 50% de prise de poids // TZD
AMG-131 : Mécanisme d’action AMG-131 Recrutement faible des co-activateurs de l’adipogénèse ex : DRIP 205 Recrutement de co-répresseurs ex : NCoR ADN Pol II PPRE PPRE Activation majoritaire de la transcription des gènes « glucidiques » Répression de la transcription des gènes
Les PPARs remis en cause ? Certaines études de carcinogenèse sembleraient montrer que sur certains modèles murins l’activation des PPARs favoriseraient le développement de certains cancers. Mais, d’autres études sur d’autres modèles sembleraient affirmer le contraire, voire parleraient de protection contre certains cancers. => Il faut être vigilant, nous avons peu de recul vis à vis de ces molécules et les études de carcinogenèse commencent à peine.
V. Conclusion • PPAR : cibles très intéressantes pour le traitement de nombreuses pathologies • Diabètes • Dyslipidémies • Inflammation et pathologies associées • MAIS ils présentent également des risques potentiels : • Localisation ubiquitaire • Implication dans un grand nombre de métabolismes • Carcinogénèse ??
Dans l’encart « PPARα » : • les protéines de la phase aiguë de l’inflammation • l’expression des CAMs endothéliales.