第五章 非经典配合物
第五章 非经典配合物. 什么是非经典配合物 : 非经典配合物 是指 : 金属和一个或多个碳原子直接键 合而形成的一类化合物 . 常见的配体是 CO, 苯 , 烯烃等 . 有人也把它们称为金属有机化合物 . 例如 :. 发展过程. Historical Perspective Zeise ’ s Salt Na[PtCl 3 C 2 H 4 ] Frankland, Zn(Et) 2 , first metal alkyl Grignard, organomagnesium halides

第五章 非经典配合物
E N D
Presentation Transcript
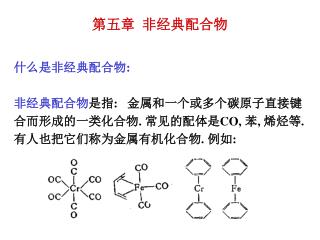
第五章 非经典配合物 什么是非经典配合物: 非经典配合物是指: 金属和一个或多个碳原子直接键 合而形成的一类化合物. 常见的配体是CO, 苯, 烯烃等. 有人也把它们称为金属有机化合物. 例如:
发展过程 • Historical Perspective • Zeise’s Salt Na[PtCl3C2H4] • Frankland, Zn(Et)2, first metal alkyl • Grignard, organomagnesium halides • Pope and Peachey, PtMe3I, first transition metal s-alkyl • 1917. Schenk, lithium alkyls • Heiber, Fe(CO)4H2 first transition metal hydride • 1951. Pauson and Miller, ferrocene • Fisher, bis arene metal complex • 1973. Fisher, Cr(CO)4(CR), first carbyne complex • 1983. Bergman, Graham, C-H bond activation • Green, Brookhart, agostic metal-hydrogen interaction
有效原子系数规则(Sidgwick, 1927) 有效原子系数(EAN)规则,有效原子系数是指中心原子 的电子数和配体给予的电子数之和,该规则认为, 中心 原子形成稳定配合物的有效原子系数应等于紧随它后 面的惰性气体的原子系数.有的经典配合物也符合, 但多数不符合. 如:
有效原子系数(EAN)规则运用到非经典配合物很有效,有效原子系数(EAN)规则运用到非经典配合物很有效, 如多数简单羰基配合物符合EAN规则, 中心原子为奇 数的羰基配合物, 容易被氧化, 还原或聚合成多核配合 物, 以尽量符合该规则. 如:
一些配体对EAN提供的电子数: EAN规则的实质是过渡金属的(n-1)d, ns, 和np共有9个价层轨道全部得到利用时, 便能达到惰性气体封闭壳层结构, EAN规则是经验规则, 有局限性, 但对合成新的配合物有一定的指导作用.
EAN规则的应用: 1), 利用EAN规则估计羰基配合物的稳定性
EAN规则的应用: 2), 利用EAN规则估计反应的方向和产物:
EAN规则的应用: 3), 利用EAN规则估算分子中存在的M-M键, 并推测它 们的结构:例如, Fe3(-CO)2(CO)10和Co4( -CO)3(CO)9 的结构. 按EAN规则Fe原子还缺2个电子, 因此每个Fe原子必须形成两个 M-M键方可达到18电子的要求; Co原子还缺3个电子, 因此每个 Co原子必须形成三个Co-Co键方可达到18电子的要求.
Fe3 (CO)12和Co4 (CO)12的结构 Fe3(-CO)2(CO)10 Co4( -CO)3(CO)9
18电子和16电子规则 EAN规则的另一种说法是18电子规则, 即不考虑中心 原子内层电子, 只考虑中心原子外层和次外层电子,中 心原子外层和次外层电子加上配体给予的电子数总和 等于18时, 则形成稳定的配合物, 此外, 还发现电子数 之和为16时也能形成稳定的配合物, 如Ir2+, Pt2+等能形 成16电子配合物. 16电子和18电子规则只是经验规则.
烯烃配合物 烯烃配合物的存在和制备: 蔡司盐是第一个烯烃配合物, 与烯烃形成配合物的主要 是具有一定数目d电子的过渡金属, 以VIII族最为典型, Cu+, Ag+, Hg2+等与烯烃生成配合物的能力也很强.
烯烃配合物的合成 1). 直接合成法:烯烃直接和金属盐或配位不饱和的非经典配合物反应, 如: Ag+ + C2H4 [Ag(C2H4)]+ [IrCl(CO)(Pph3)2] + R2C=CR2 [IrCl(CO)(pph3)2(R2C=CR2)] 2). 取代反应:烯烃取代其它配体, 如卤素, 羰基, 或其 它烯烃. K2[PtCl4] + C2H4 K[PtCl3(C2H4)]·H2O + KCl [(C2H4)2Pt2Cl4] + 2CH3CH=CH2[(CH3CH=CH2)2Pt2Cl4] + 2C2H4
烯烃配合物的结构 根据烯烃配合物的结构, 可以分为两类, 具有平面正方 形或八面体结构的, 称为S类, 具有平面三角形或三角 双锥结构的, 称为T类, 炔烃的配合物和烯烃相似. 例:
烯烃配合物的结构 属S类的金属有Pt(II), Pd(II), Fe(II), Rh(I), Re(I)等, 属 T类的金属有Pd(0), Pt(0), Fe(0), Ir(I), W(I), Mo(I)等, 属S类的金属配合物的氧化态较T类高, 所具有的d电子 数较少. S类配合物 T类配合物 双键比配位前增长2-4pm 双键比配位前增长15-17pm 双键与PtX3平面接近垂直 双键与PtXn平面接近平行 Pt配合物IR收缩振动频率 配合物IR收缩振动频率比自 比自由双键减少140cm-1, 由三键减少约500cm-1. 三键减少约250cm-1.
蔡司盐中金属与烯烃间的协同成键过程: 这种配位键和反馈键的协同作用使得蔡司盐有相当 的稳定性.
炔烃配合物: 三键垂至于分子平面, t-Bu基团往外弯曲~20o.
由于炔烃中有两套相互垂直的键和*键配合物, 它们 可以形成多核配合物, 如:
配位烯烃和亲核剂的反应 烯烃配位后易受到亲核试剂的进攻,配位烯烃和亲核剂 的反应是一类重要的反应.如Pd2Cl4(C2H4)2与醇的反应:
配位烯烃和亲核剂的反应 亲核试剂进攻烯烃的难易程度与金属及烯烃的性质有关, 取决于键和键两组分贡献的大小. 以d8金属为例: Ru(0), Rh(I), Pd(II)和烯烃生成反馈键的能力依次减弱: Ru(0)>Rh(I)>Pd(II), Ru(0)的激发能较低, 说明容易回授 电子给烯烃, 致使配位烯烃和亲核试剂反应的能力减弱.
烯丙基型配合物 • 烯丙基型配合物的键型 烯丙基与金属以两种形式成键, 一种是以键和金属配 位, 另一种是以三电子与金属形成离域键, 两种键型能 互相转化.
下列的烯丙基配合物就是通过型转变而来.下列的烯丙基配合物就是通过型转变而来.
烯丙基型配合物 2. 烯丙基型配合物的性质及重要反应 单一配体的烯丙基配合物一般由烯丙基合镁的卤化物 (Grinard试剂) 与 金属氯化物或溴化物在乙醚中制得.
2. 烯丙基型配合物的性质及重要反应 烯丙基配合物是通过碳键合金属直接相连, 而金属碳键 通常不稳定, 烯丙基配合物性质非常活泼, 其稳定性随 过渡金属原子序数增加而递增, 同族元素有如下顺序: Ni<Pd<Pt, Cr<Mo<W, Ti<Zr<Hf. 一般说来, 中心原子 电子数为偶数时烯丙基配合物比为奇数时更稳定.
配位烯烃和亲核剂反应的应用 烯烃和炔烃的配合物又称为-配合物, 它们在工业上有 重要的应用, 这主要和不饱和烃的氧化, 氢化, 聚合等 反应的催化有关, 如直接氧化法自乙烯生产乙醛: PdCl2为催化剂, CuCl2为助催化剂, 氧气或空气为氧化剂.
配位烯烃和亲核剂反应的应用 二(1-3--烯丙基)合镍参加的反应: