แรงกระทำระหว่างโมเลกุล (Intermolecular Forces)
แรงกระทำระหว่างโมเลกุล (Intermolecular Forces). เนื้อหาที่จะเรียน. 1 Intermolecular Forces and some Properties of Liquids 2 Vaporization of Liquids: Vapor Pressure 3 Some Properties of Solids 4 Phase Diagrams 5 Van der Waals Forces 6 Hydrogen Bonding


แรงกระทำระหว่างโมเลกุล (Intermolecular Forces)
E N D
Presentation Transcript
แรงกระทำระหว่างโมเลกุล (Intermolecular Forces)
เนื้อหาที่จะเรียน 1 Intermolecular Forces and some Properties of Liquids 2 Vaporization of Liquids: Vapor Pressure 3 Some Properties of Solids 4 Phase Diagrams 5 Van der Waals Forces 6 Hydrogen Bonding 7 Network Covalent Solids and Ionic Solids
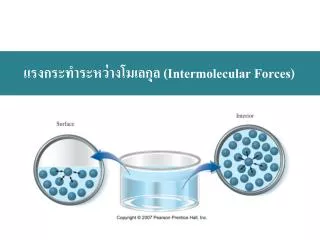
Intermolecular Forces and Some Properties of Liquids • Cohesive Forces • Intermolecular forces between like molecules. • Adhesive Forces • Intermolecular forces between unlike molecules. • Surface Tension • Energy or work required to increase the surface area of a liquid. • Viscosity • A liquids resistance to flow
Boiling Point Mercury manometer Vapor pressure of liquid Pvap independent of Vliq Pvap independent of Vgas Pvap dependent on T
The Critical Point • ความหนาแน่นของของเหลวลดลงแต่ของไอจะเพิ่มขึ้นและต่อมาจะมีค่าเท่ากัน • แรงตึงผิวของของเหลวจะเข้าใกล้ศูนย์ ชั้นของของเหลวและไอจะกลายเป็นหนึ่งเดียว • ไม่เห็นความแตกต่าง
ตัวอย่างการใช้ข้อมูลความดันไอตัวอย่างการใช้ข้อมูลความดันไอ จากปฏิกิริยาเคมีชนิดหนึ่งได้ผลิตภัณฑ์เป็นน้ำมวล 0.132 g ที่อุณหภูมิ 50.0 oC ในภาชนะปิดปริมาตร 525 mL จงทำนายว่าน้ำนี้จะอยู่ในสถานะ (a) liquid only (b) vapor only (c) liquid-vapor equilibrium
ΔHvap P2 1 1 ln = - ( - ) P1 T1 T2 R 1 ln P = -A ( ) + B T ΔHvap A = R Clausius-Clapeyron Equation
Some Properties of Solids Freezing Point Melting Point ΔHfus(H2O) = +6.01 kJ/mol
Sublimation ΔHsub = ΔHfus + ΔHvap = -ΔHdeposition
Phase Diagrams Iodine
Phase Diagrams Carbon dioxide
Interpreting a Phase Diagram General Chemistry: Chapter 12
Van der Waals Forces • Instantaneous dipoles. • Electrons move in an orbital to cause a polarization. • Induced dipoles. • Electrons move in response to an outside force. • Dispersion or London forces. • Instantaneous dipole – induced dipole attraction. • Related to polarizability.
Instantaneous and Induced Dipoles < 10 kJ/mol
Dipole Dipole Interactions 5 to 20 kJ/mol
Electrostatic Potential Maps General Chemistry: Chapter 12
ความสัมพันธ์ระหว่างแรงกระทำระหว่างโมเลกุลกับสมบัติของสารประกอบความสัมพันธ์ระหว่างแรงกระทำระหว่างโมเลกุลกับสมบัติของสารประกอบ จุดเดือดที่พบจริง CCl4= 349.9 K ClNO= 266.7 K Cl2= 239.1 K N2 = 77.3 K เรียงลำดับจุดเดือดของสารต่อไปนี้: CCl4, Cl2, ClNO, N2.
Hydrogen Bonding 15 to 40 kJ/mol
Hydrogen Bonding in Water around a molecule in the solid in the liquid
Ion-dipole Interactions cation-p Interactions
anion-p Interactions p-p Interactions
End of Chapter Questions • You can think about problems in reverse to help sort out a strategy. a b If I had the answer, what would I have used to get it. c