Reacciones REDOX
Reacciones REDOX. Prof. Sergio Casas-Cordero E. Introducción. Sobre el alambre de cobre se deposita plata metálica y, a la vez, el cobre se disuelve, dando a la solución el color azul. Video 01. Nuevo tipo de reacción: Reacción de transferencia de electrones. Algunas Definiciones:.

Reacciones REDOX
E N D
Presentation Transcript
Reacciones REDOX Prof. Sergio Casas-Cordero E.
Introducción. Sobre el alambre de cobre se deposita plata metálica y, a la vez, el cobre se disuelve, dando a la solución el color azul. Video 01 prof. S. Casas-Cordero E.
Nuevo tipo de reacción: Reacción de transferencia de electrones prof. S. Casas-Cordero E.
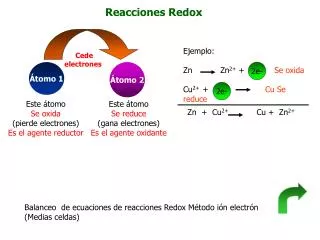
Algunas Definiciones: Oxidación:Proceso en el que una sustanciapierde electrones. Reducción: Proceso en el que una sustanciaganaelectrones. Agente Oxidante:Sustancia que provoca la oxidación y se reduce. Agente Reductor:Sustancia que provoca la reducción y se oxida. prof. S. Casas-Cordero E.
Oxidación: Cuando un átomo neutro pierde uno o más electrones, se transforma en un catión. M(s) Mn+ + ne1- Cuando un anión pierde electrones, puede transformarse en un átomo neutro o en un catión. Xn- X + ne1- Xn- X1+ + ne1- prof. S. Casas-Cordero E.
Reducción: Son procesos contrarios a la oxidación, por lo cual, las ecuaciones anteriores escritas de modo inverso, representan “reducción” Mn+ + ne1- M(s) X + ne1- Xn-ganancia de electrones prof. S. Casas-Cordero E.
Otro ejemplo de reacción redox Cu (s)+ 4 HNO3 (ac) Cu(NO3)2 (ac)+ 2 NO2 (g)+ 2 H2O(l) ¿Cómo se reconoce que es una ecuación de oxidación - reducción? Video - 02 prof. S. Casas-Cordero E.
Cambios ocurridos en el valor del EO oxidación (agente reductor) - + 0 reducción (agente oxidante) prof. S. Casas-Cordero E.
Estados de oxidación (EO) • Carga que el átomo tendría si todos sus enlacesfueran considerados completamenteiónicos, asignando los pares de electrones enlazantes al átomo más electronegativo. • Excepto para iones monoatómicos, el número de oxidación para un átomo NOrepresenta su carga eléctrica real. prof. S. Casas-Cordero E.
Se calcula por: EO = (e-V – e- totales en la Estruc. de Lewis) prof. S. Casas-Cordero E.
Consideremos como ejemplo el ácido Nítrico, HNO3 prof. S. Casas-Cordero E.
Cantidad de e-V:O = 6 e-vN = 5 e-vH = 1 e-v Ya que ENH < ENN < ENO Los Estados de Oxidación serán: O = (6 – 8) = -2N = (5 – 0) = +5H = (1 – 0) = +1 prof. S. Casas-Cordero E.
Guías para determinar EO 1. Átomo en un elemento puro: EO igual a 0. 2.Iones monoatómicos: EO igual a la carga del ion. 3.Flúor: EO = -1 en cualquier compuesto. 4.EO(H)= +1 y EO(O)= -2 mayoría compuestos 5. Cl, Br y I: EO siempre -1, excepción con O presente 6. La suma algebraicade los EO debe ser igual a la carga neta de la molécula. prof. S. Casas-Cordero E.
0 +1 5 -2 +2 5 -2 4 -2 +1 -2 Cu (s) + 4 HNO3 (ac) Cu(NO3)2 (ac) + 2 NO2 (g) + 2 H2O (l) Aplicación de los conceptos: El cobre se oxida; aumentasu EO El ácido nítrico se reduce; el EO (N) disminuye. Agente reductor : Cu Agente oxidante : HNO3continuar prof. S. Casas-Cordero E.
Agentes comunes oxidantes y reductores prof. S. Casas-Cordero E.
Otro ejemplo: OXIDACIÓN peróxido EO = +7 EO = -1 EO = 0 EO = +2 Video 03 REDUCCIÓN prof. S. Casas-Cordero E.
Calcular el EO del átomo marcado con la flecha: a) HNO2 b) HC2O41- c) (NH4)2Cr2O7 d) H3BO3 Solución a):EOH + EON + 2xEOO = 0 X = +3 (+1) + X + 2x(-2) = 0 Solución b):EOH + 2xEOC + 4xEOO = -1 (+1) + 2xX + 4x(-2) = -1 X = +3 Solución c):El ión amonio es NH41+ , luego:2x(+1) + 2xEOCr + 7xEOO = 0 X = +6 2x(+1) + 2xX + 7x(-2) = 0 Solución d):3xEOH + EOB + 3xEOO = 0 X = +3 3x(+1) + X + 3x(-2) = 0 prof. S. Casas-Cordero E.
Balanceo de ecuaciones redox 1. Reconocer la reacción como un proceso redox. 2. Separar el proceso en semirreacciones. 3. Hacer el balance de masa para cada semirreacción. 4. Hacer el balance de carga para cada semirreacción. 5. Igualar los electrones transferidos, multiplicando cada semirreacción por un factor apropiado. 6. Sumar las semirreacciones para obtener la ecuación neta balanceada. prof. S. Casas-Cordero E.
Medio ácido: 1. Dividir la ecuación en dos semirreacciones; oxidación y reducción 2. Igualar el átomo que cambia su EO 3. Los átomos de oxígeno se igualan con moléculas de agua. Los átomos de Hidrógeno con ión H1+. 4. Colocar el total de electrones transferidos 5. Multiplicar por factor que permita igualar este total de electrones y sumar ambas semirreacciones 6. Simplificar al máximo posible prof. S. Casas-Cordero E.
Ejemplo:Cu(s) + HNO3(ac) Cu2+(ac) + NO2(g) prof. S. Casas-Cordero E.
Otro ejemplo: +6 +2 0 -1 HS2O31-(ac) + I2(ac) SO42- + I1-(ac) HS2O31- + 5 H2O 2 SO42- + 11 H1+ + 8 e- x 1 Oxidación + x 4 Reducción I2 + 2 e- 2 I1- HS2O31- + 5 H2O + 4 I2 2 SO42- + 11 H1+ + 8 I1- prof. S. Casas-Cordero E.
Medio básico: 1. Dividir la ecuación en dos semirreacciones; oxidación y reducción 2. Igualar el átomo que cambia su EO 3. Colocar el total de electrones transferidos 4. La carga eléctrica se iguala con aniones Hidróxido, OH1-. Los átomos de Oxígeno se igualan con moléculas de agua 5. Multiplicar por factor que permita igualar este total de electrones y sumar ambassemirreacciones 6. Simplificar al máximo posible(ver ejemplo) prof. S. Casas-Cordero E.
Otra forma para el medio básico… 1. Dividir la ecuación en dos semirreacciones; oxidación y reducción 2. Igualar el átomo que cambia su EO 3. Por cada Oxígeno en exceso, añadir una molécula de H2O en el mismo lado y 2 OH1- al lado contrario. 4. Colocar el total de electrones transferidos 5. Multiplicar por factor que permita igualar este total de electrones y sumar ambas semirreacciones 6. Simplificar al máximo posible(ver ejemplo) prof. S. Casas-Cordero E.
Ejemplo:Cr(OH)3 + Cl2 CrO42- + Cl1- • Se determinan los EO de cada átomo: Cr(OH)3 + Cl2 CrO42- + Cl1- +3 -2 +1 0 +6 -2 -1 • reducción • oxidación prof. S. Casas-Cordero E.
(MB)Cr(OH)3 + Cl2 CrO42- + Cl1- prof. S. Casas-Cordero E.
+3 +2 Fe2+ Fe3+ +6 +3 Cr2O72-Cr3+ Balances redox en forma iónica ¿Como se balancea una reacción en la que se oxida el Fe2+ a Fe3+ mediante Cr2O72- en una solución ácida? • Escribir la ecuación sin balancear en forma iónica. Fe2+ + Cr2O72- Fe3+ + Cr3+ • Separar la ecuación en dos semireacciones. Oxidación: Reducción: • Balancear por inspección todos los elementos que no sean ni oxígeno ni hidrógeno en las dos semireacciones. Cr2O72- 2Cr3+
Para reacciones en medio ácido, agregar H2O para balancear los átomos de O y H+ para balancear los átomos de H. Cr2O72- 2 Cr3+ + 7 H2O 14 H1+ + Cr2O72- 2 Cr3+ + 7 H2O • Agregar electrones en el lado apropiado de cada una de las semireacciones para balancear las cargas. Fe2+ Fe3+ + 1e- 6e- + 14 H1+ + Cr2O72- 2 Cr3+ + 7 H2O • Si es necesario, igualar el número de electrones en las dos semireacciones multiplicando cada una de las reacciones por un coeficiente apropiado. 6Fe2+ 6 Fe3+ + 6e- 6e- + 14H+ + Cr2O72- 2Cr3+ + 7H2O
Unir el lado izquierdo de una semireacción con el lado izquierdo de la otra y el derecho con el derecho y eliminar lo que sea posible. El número de electrones en ambas partes debe cancelarse. 6 Fe2+ 6 Fe3+ + 6 e- Oxidación: 6 e- + 14 H1+ + Cr2O72- 2 Cr3+ + 7 H2O Reducción: 14 H1+ + Cr2O72- + 6 Fe2+ 6 Fe3+ + 2 Cr3+ + 7 H2O • Verificar que el número de átomos y las cargas estén balanceadas. 14x1 – 2 + 6x2 = 24 = 6x3 + 2x3 • Para reacciones en solución básica, agregar (OH1-) en ambos lados de la ecuación por cada H+ que aparezca en la ecuación. 14 H1+ + 14 OH1- + Cr2O72- + 6 Fe2+ 6 Fe3+ + 2 Cr3+ + 7 H2O + 14 OH1- 14 H2O + Cr2O72- + 6 Fe2+ 6 Fe3+ + 2 Cr3+ + 7 H2O + 14 OH1- 7 H2O + Cr2O72- + 6 Fe2+ 6 Fe3+ + 2 Cr3+ + 14 OH1-
Electroquímica Prof. Sergio Casas-Cordero E.
Electroquímica: Es una rama de la química que estudia la transformación entre la energía eléctrica y la energía química. Estudia las reacciones químicas que se dan en la interfase de un conductor eléctrico (llamado electrodo, que puede ser un metal o un semiconductor) y un conductor iónico (el electrolito) pudiendo ser una disolución y en algunos casos especiales, un sólido. prof. S. Casas-Cordero E.
Electroquímica Existen dos tipos de transformaciones electroquímicas: • Rx. Electrolíticas o electrólisis: Son aquellas reacciones químicas que ocurren mediante una diferencia de potencial aplicada externamente. • Rx. Galvánica: Son aquellas donde la caída de potencial eléctrico, es creada como consecuencia de la misma reacción, por lo cual suelen ser conocidas como "acumuladores de energía eléctrica, baterías o pilas“. prof. S. Casas-Cordero E.
Componentes de los dispositivos electroquímicos • Ánodo: electrodo en donde ocurre la oxidación. Signo negativo. • Cátodo: electrodo en donde ocurre la reducción. Signo positivo. • Electrolito: sustancia soluto que se encuentra en forma de iones en una solución acuosa o fundido prof. S. Casas-Cordero E.
Potencial Estándar, Eº: • Potencial estándar: potencial de una pila medido a 25 °C, 1 atm y en concentraciones 1 M de todos los solutos • Potencial estándar de Hidrógeno: valor de referencia, considerado como cero volts (0 V) y que se basa en cualquiera de las reacciones del Hidrógeno; H2(g) 2 H1+(ac) + 2e1- (oxidación) 2 H1+(ac) + 2e1- H2(g) (reducción) prof. S. Casas-Cordero E.
Rx espontánea Zn – Cu - limón prof. S. Casas-Cordero E.
Los potenciales de diferentes sustancias se miden en función del Potencial estándar del Hidrógeno. • Potencial REDOX (E°redox): Suma de Potenciales de Reducción y Oxidación. E°redox = E°red + E°ox Criterio IUPAC: ∆Eº = Eº red(derecha) – Eº red(izquierda) prof. S. Casas-Cordero E.
Midiendo Potencial de una Rx prof. S. Casas-Cordero E.
Ejemplos de Potenciales de reducción Estándar prof. S. Casas-Cordero E.
Criterio de Espontaneidad: • Si al combinar la semi - ecuación de reducción con una semi - ecuación de oxidación, se obtiene un Potencial Redoxpositivo, la reacción es espontánea. • Si el Potencial resultante es negativo, la reacción es no espontánea. prof. S. Casas-Cordero E.
Toda reacción química que resulte no espontánea, si se invierte, será espontánea. Ej. Cu(s) + Fe2+(ac) Cu2+(ac) + Fe(s) Fe2+(ac) + 2e1- Fe(s) E°red = - 0,44 Cu(s) Cu2+(ac) + 2e1-E°ox = - 0,34 E°redox = (-0,44) + (-0,34) = -0,78 No espontánea prof. S. Casas-Cordero E.
Invirtiendo la reacción, resulta: Cu2+(ac) + Fe(s) Cu(s) + Fe2+(ac) Cu2+(ac) + 2e1- Cu(s) E°red = +0,34 Fe(s) Fe2+(ac) + 2e1-E°ox = +0,44 E°redox = (+0,34) + (+0,44) = +0,78 Espontánea prof. S. Casas-Cordero E.
Pila electrolítica consume el trabajo eléctrico de una fuente de energía externa, para realizar una reacción no espontánea. (ver ejemplo siguiente) prof. S. Casas-Cordero E.
Obtención de Sodio puro desde NaCl fundido prof. S. Casas-Cordero E.
(otro ejemplo)Cromado electrolítico de Cobre prof. S. Casas-Cordero E.
Pila electrolítica para purificar el CobreCátodos de Cobre prof. S. Casas-Cordero E.
Reacciones involucradas: • Reducción: Cu2+(ac) + 2 e1- Cu(s) Oxidación: H2O 2 H1+(ac) + ½ O2(g) + 2 e1- prof. S. Casas-Cordero E.
Electrólisis del Agua prof. S. Casas-Cordero E.
La Reacción: H2O(l) H2(g) + ½ O2(g) Oxidación: O2- ½ O2(g) + 2 e- Reducción: 2 H1+ + 2 e- H2(g) prof. S. Casas-Cordero E.