Polyarthrite rhumatoïde
Polyarthrite rhumatoïde. Rhumatisme inflammatoire le plus fréquent (0.5-1 %) Cause inconnue, multi-factorielle Le plus sévère: atteinte fonctionnelle, surmortalité Prédominance féminine (4/1) Sujet jeune: 35-55 ans, formes juvéniles

Polyarthrite rhumatoïde
E N D
Presentation Transcript
Polyarthrite rhumatoïde • Rhumatisme inflammatoire le plus fréquent (0.5-1 %) • Cause inconnue, multi-factorielle • Le plus sévère: atteinte fonctionnelle, surmortalité • Prédominance féminine (4/1) • Sujet jeune: 35-55 ans, formes juvéniles • Atteinte distale, symétrique, destructrice, polyarticulaire • HLA DRB1*0401, 0404, 0101 • Facteurs rhumatoïdes (70 %), • Ac anti-fillagrine ou anti-CCP peptides cycliques citrullinés (très spécifiques)
Polyarthrite rhumatoïde • Affection de longue durée (prise en charge à 100 %) • 200.000 cas en France; 4500 nouveaux cas / an • Réduction de durée de vie de 5 à 10 ans • Si vascularite, mortalité superposable à celle du cancer du colon • Coût socio-économique considérable car sujets jeunes • Retentissement professionnel, familial
Immunopathologie de la PR • Accumulation de lymphocytes Th1 • Production de cytokines pro-inflammatoires • Défaut de cytokines anti-inflammatoires • Destruction >> réparation • Prolifération incontrollée des synoviocytes • Défaut d’apoptose • Mutations secondaires de p53
Interactions cellulaires et maladies Cellules pathogènes IL-23 T cells IFN- IL-17 IL-18 IL-15 IL-12 IL-1 TNF- Cellules mésenchymateuses Monocytes APC Destruction Cytokines Enzymes
Interactions cellulaires et maladies Cellules pathogènes IL-23 Lymphocytes T IFN- IL-17 IL-18 IL-15 IL-12 IL-1 TNF- Cellules mésenchymateuses Monocytes Lymphocytes B Cellules présentatrices d’antigène Cytokines Enzymes Destruction
Interactions cellulaires et régulation Lymphocytes Th1 pathogènes IFN- IL-23 IL-17 IL-18 Destruction IL-1 TNF- IL-12 C mésenchymateuses Monocytes IL-1-Ra Récepteurs solubles IL-10 Réparation TGF- IL-4 Lymphocytes Th2 protecteurs
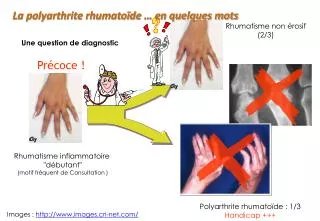
Polyarthrite rhumatoïde • Deux grands tableaux Tardif Précoce Diagnostic puis traitement Traitement
Polyarthrite rhumatoïde:signes précoces • Raideur matinale • Douleurs nocturnes • Syndrome du canal carpien • Relative symétrie • Caractère permanent • Synovites des poignets et MCP • Ténosynovite des fléchisseurs
Polyarthrite rhumatoïde:diagnostic différentiel • Rhumatisme inflammatoire bénin intermittent Arthralgies migratrices, transitoires et non destructrices • Syndrome de Gougerot-Sjögren Signes d’accompagnement: syndrome secFR, AAN moucheté • Connectivites Signes d’accompagnement extra-articulaires AAN • Spondylarthropathies Asymétrie Atteinte axiale HLA-B27 • Si mono-arthrite: infection à éliminer
Polyarthrite rhumatoïde:évolution radiologique • Deux grands tableaux Tardif Précoce
Signes extra-articulaires • Syndrome de Raynaud • Syndrome de Gougerot-Sjogren • Atteinte pulmonaire • Vascularite • Neuropathie • Nodules rhumatoïdes
Les Arthrites Juvéniles Idiopathiques • Formes systémiques (ancienne maladie de Still) fièvre le soir avec hyperleucocytose signes cutanés signes articulaires • Formes oligoarticulaires 3 articulations, surtout genou petite fille 4 ans garçon 10-12 ans, HLA B27 • Formes polyarticulaires avec ou sans signes systémiques • Dans tous les cas surveiller les yeux anticorps anti-nucléaires rééducation
Traitement de la Polyarthrite Rhumatoïde • Traitement symptomatique antalgiques anti-inflammatoires non stéroïdiens corticoïdes • Traitement de fond: classique: sels d’or, anti-paludéens, thiolés, salazopyrine méthotrexate leflunomide cyclosporine, cyclophosphamide inhibiteurs des cytokines • Traitement local infiltrations, synoviorthèses synovectomies remplacement articulaire
Traitement précoce de la PR • Bon sens général • Principe de base en cancérologie • Extension aux maladies rétro-virales • Destruction articulaire en 2 ans • Reconstruction d’une articulation illusoire • Anomalies moléculaires secondaires
Limites au traitement précoce • Diagnostic difficile • Faiblesse des marqueurs diagnostiques • Faiblesse des marqueurs pronostiques • Mauvaise corrélation inflammation et destruction • Médicaments actuels insuffisants
Marqueurs pronostiques et PR • Critères de l’ACR trop tardifs car diagnostic de certitude • Vitesse de progression radiologique mais élément cinétique tardif • Taux de facteurs rhumatoïdes mais spécificité imparfaite • Sous-types HLA-DR 4 0404, 0401
Nouveaux marqueurs pronostiques et PR • Anticorps anti-kératine (fillagrine), • Anticorps anti-CCP (peptides citrullinés) • Polymorphisme gènes TNF, IL-1a, IL-1b et gravité • Polymorphisme gènes IL-4 et protection • Auto-anticorps anti-cytokines (IL-1 et protection • Séquençage du génome humain • Pharmacogénomique et réponse au traitement • Concordance chez jumelles homozygotes: 17.5 %
Méthotrexate en Rhumatologie • Polyarthrite rhumatoïde • Arthrite chronique juvénile • Rhumatisme psoriasique • Spondylarthropathies • Vascularites: Horton, Wegener, … • Connectivites: myosites, lupus, sclérodermie, Gougerot-Sjögren
Méthotréxate et polyarthrite rhumatoïde • Traitement de fond le plus utilisé • Bon rapport efficacité / intolérance • Meilleur taux de maintenance • Rareté des rémissions • Effet suspensif • Effet incertain sur la dégradation • Effets secondaires
Mode d’action du Méthotrexate • Inhibition de la dehydrofolate reductase • Désactivation des monocytes/macrophages • Inhibition de la production des cytokines proinflammatoires et induction de la production des cytokines anti-inflammatoires • Induction de la production d’adénosine • Induction d’une apoptose des lymphocytes T activés
Méthotréxate et polyarthrite rhumatoïde • Posologie: 10 mg/semaine (7.5-25) en une prise • Voie: IM > per os (AMM) • Surveillance biologique mensuelle: NFS, plaquettes, VS, transaminases, créatinine • Surveillance pulmonaire avant début puis 1/an RP, EFR, gaz du sang • Contraception obligatoire
Effets secondaires graves du Méthotréxate • Effet direct: toxique ou allergique • Effet indirect, lié au mode d’action • Hématologiques: terrain, médicaments (Bactrim) • Pulmonaires: infections opportunistes hypersensibilité • Lymphomes: incidence spontanée PR x 5, SGS x 40 rôle de EBV, IL 10
Insuffisance d’efficacité du Méthotréxate • Augmenter la tolérance (A.folique, Speciafoldine) • Augmenter la dose (20 mg/s ou >) • Changer de voie d’administration (IM) • Associer une corticothérapie • Changer de traitement de fond • Envisager les associations de traitements de fond et les biothérapies
Mode d’action du Léflunomide • Métabolite hépatique actif A77 1726 • Inhibiteur non compétitif de la dihydro-orotate-deshydrogenase (voie des pyrimidines), de la synthèse d’ARN, d ’ADN et de la prolifération cellulaire (p53, p21) • Action plus nette sur les cellules à cycle cellulaire rapide (lymphocytes T et B activés) • Inhibition de NFkB et de la production des cytokines proinflammatoires (TNF, IL-1) et des protéases • Induction des inhibiteurs IL-1Ra et TIMP
Léflunomide (Arava) • Dose de charge: 100 mg/j x 3 per os • Entretien: 1 cp à 20 mg/j • Surveillance biologique mensuelle: NFS, plaquettes, VS, transaminases, créatinine • Effets secondaires digestifs hépatiques cutanés • Contraception nécessaire
Associations de traitements de fond • Principe de base de la chimiothérapie, VIH • Recherche d’un effet additif ou synergique • Réduction de la toxicité individuelle • Action sur une ou différentes cibles cellulaires: - monocytes: MTX, SLP - lymphocytes T: CSA - purines MTX; pyrimidines: Léflunomide • Extension aux approches spécifiques anti-TNF/IL-1
Association de traitements de fond classiques • Principes des associations: Cibles cellulaires différentes Association en un ou deux temps Toxicité supplémentaire acceptable • MTX +CSA > MTX (+ 25 %) Effet protecteur articulaire possible Néoral: Dose: 2.5 à 5 mg/kg en deux prises Surveillance: TA, fonction rénale • Salazopyrine, plaquenil, methotrexate: Association la mieux étudiée Toxicité supplémentaire réduite
Modulation de l’action du TNFa Remicade Humira Anticorps anti-TNF R p55 soluble / TNF a LT a a R TNF p55 a R TNF R p75 soluble p75 Cible Enbrel Effets biologiques
Inhibiteurs du TNFa • Infliximab ou Remicade: anticorps chimérique anti-TNF 3 mg/kg perfusion iv sur 2 h, associé au méthotrexate S0, S2, S6 puis S8 • Adalimumab ou Humira: anticorps humain anti-TNF 40 mg s/c toutes les 2 semaines, associé au méthotrexate • Etanercept ou Enbrel: récepteur soluble p75 2x25 mg/semaine s/c • Effets secondaires intolérance infections (tuberculose: IDR, RP) signes neurologiques centraux
Tuberculose et inhibiteurs du TNFa • Effet des anti-TNF sur la structure des granulomes avec risque de diffusion. • Augmentation du risque au cours des maladies inflammatoires • Prévention: Interrogatoire IDR RP avec scanner si doute Surveillance prolongée • Si suspicion Bithérapie (Rifinah, 2 cp/j)pendant 3 mois Début anti-TNF après un mois
Type II IL-1R soluble Modulation de l’action de l’IL-1 Type I IL-1R soluble IL-1 Type II IL-1R soluble Protéine Accessoire AcP Type I IL-1R IL-1 Anakinra Kineret IL-1RA Type II IL-1R Activation gènique
Inhibiteurs de l’IL-1 • Anakinra ou Kineret: Antagoniste du récepteur de l’IL-1 100 mg/jour s/c Associé au méthotrexate Surveillance: NFS • Effets secondaires intolérance cutanée aux points d’injection neutropénie infections (bactériennes)
Traitement local précoce et pronostic • Traitement local associé au traitement général, sans le remplacer • Infiltrations, synoviorthèses • Synovectomies précoces + synoviorthèses • Arthroscopique ou chirurgicale • Poignet, genou, épaule • Remplacement articulaire • Importance de la concertation
Conclusion • Traitement symptomatique au tout début (AINS, antalgiques) sans doses élevées de corticoïdes • Traitement de fond précoce (MTX) dès forte suspicion • Association de traitements si réponse insuffisante • Informer dès le début et ensuite encore • Dire qu’il n’y a plus de fauteuil roulant • Discuter rapidement de la génétique en donnant des chiffres • Faire tout pour le maintien dans la vie économique • Ne rien interdire, favoriser le sport, la natation
Stade du diagnostic non posé • Arthralgies migratrices • Arthrites intermittentes • Examen clinique sensiblement normal • Traitement symptomatique (AINS, antalgiques) • Pas de corticoïdes • A revoir dans 3 mois • Si persistance, début d’un traitement de fond (MTX sinon Plaquenil)
Stade de PR au début • Arthrites chroniques distales • Ténosynovites des extenseurs ou fléchisseurs • Examen clinique évocateur • Poursuite du traitement symptomatique (AINS, antalgiques) • Méthotrexate 7.5-10 mg/semaine • Arava 20 mg/j • Surveillance biologique, contraception • Information • Revoir à 3 mois
Stade de PR au début, réponse favorable • Vie sensiblement normale • VS/CRP normale • Examen clinique normal • Diminuer puis arrêter le traitement symptomatique (AINS, antalgiques) • Méthotrexate 7.5 mg/semaine pendant environ 18 mois • Diminuer de 2.5 mg tous les 6 mois jusqu’à arrêt • Surveillance prolongée car récidive toujours possible
Stade de PR au début, réponse insuffisante • Persistance ou régression partielle des signes • Nouvelles localisations • Poursuite du traitement symptomatique (AINS, antalgiques) • Augmenter Méthotrexate de 7.5 mg/semaine à 20 mg/s • Revoir à 3 à 6 mois
Stade de PR réfractaire • Persistance ou régression partielle des signes • Nouvelles localisations • Poursuite du Méthotrexate à haute dose • Considérer les associations • Association au Cortancyl, 10 mg/j • Association au Remicade, Enbrel, Humira • Traitement expérimental hors AMM: CTLA4-Ig, anti-CD20