Syror och baser
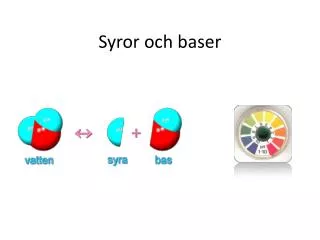
Syror och baser. Behyar Bahrami, Husbygårdsskolan, Kista – www.lektion.se. Syrors egenskaper. Alla syror är sura. De innehåller grundämnet Väte ( H ) = Hydrogen Det finns svaga syror och starka syror.


Syror och baser
E N D
Presentation Transcript
Syror och baser Behyar Bahrami, Husbygårdsskolan, Kista – www.lektion.se
Syrors egenskaper • Alla syror är sura. • De innehåller grundämnet Väte ( H ) = Hydrogen • Det finns svaga syror och starka syror. • Exempel för svaga syror är: citronsyra (i citroner), äppelsyra (I äpplen), vinsyra (i Vindruvor) och ättiksyra • Vissa läkemedel och febernedsättande tabletter t.ex. alvedon,Treo och Magnecyl innehåller en sorts syra som heter acetylsalicylsyra. • Man använder svaga syror vid matlagning. • Experiment / recept sid.38
Svaga syror och karies • När vi äter sötsaker, omvandlas sockret i munhålan så att det bland annat bildas svaga syror. Dessa svaga syror tillsammans med bakterier ger upphov till karies i tänderna.
Starka syror • På laborationer och inom industrin tillverkas och förbrukas många starka syror. De vanligaste starka syror är saltsyra (HCl),svavelsyra (H2SO4) och salpetersyra (HNO3). Alla dessa är starkt sura och mycket frätande på hud och kläder. Man använder svavelsyra bl.a. i bilbatterier. • OBS: vid spädning av starka syror, ska man hälla syran i vatten (SIV) och inte tvärtom.
Klor • Klor är en av beståndsdelarna i saltsyra. Den är en tung, gulgrön och mycket giftig gas. Under det första världskriget användes den som stridsgas. • Denna gas har viktiga egenskaper bland annat bakteriedödande och blekande.
Basiska ämnen • Baser ingår bland annat i rengöringsmedel som tvål, diskmedel och schampo. • De flesta baserna är fasta ämnen t. ex. kalk och natrium. När de löses i vatten får man en basisk lösning. Många baser är frätande. Därför måste man vara försiktig när man handskas med baser. • Exempel för baser är ammoniak och kalkvatten.
Vanliga baser • Exempel för vanliga baser är ammoniak, natriumhydroxid (kaustik soda), kalkvatten och natriumkarbonat. • Ammoniak används bl.a. när kvinnor ska färga håret. • Natriumhydroxid används vid framställning av tvål.
pH-värdet är ett mått på surheten • För att få ett mått på hur sur en lösning är, har man infört något som kallas pH-värde. Ju lägre pH-värdet är, desto surare är lösningen. Rent vatten är neutralt och har pH-värdet 7. • Sura lösningar har ett pH-värde som är mindre än 7 • Basiska lösningar har ett pH-värde som är större än 7 • Neutrala lösningar har pH-värdet 7 • Experiment sid. 48
PH- skala • 8-14 Basisk (Alkali ) Ph-värde 14 är mycket basisk • 7: Neutral • 0-6: Sur (Acid ) Ph-värde 0 är mycket sur
pH- skala basisk neutral sur 14 1 7
Indikatorer • Man kan inte enbart genom att se eller lukta på en lösning avgöra om lösningen är sur eller basisk man måste ta hjälp av andra ämnen som kallas för indikatorer. • Med en indikator kan man ta reda på om en lösning är sur, basisk eller neutral. • Vanliga indikatorer är lackmuspapper, fenolftalein och BTB (bromtymolblått
NEUTRALA LÖSNINGAR • Om man blandar en sur och en basisk lösning i lämpliga mängder, får man en lösning som varken är sur eller basisk. En sådan lösning kallas neutral. • Experiment sid.49
Försurning av naturen Den olja som används i värmepannor och dieselmotorer innehåller en viss mängd svavel. Vid förbränning av sådan olja bildas bl.a. svaveldioxid (SO2), som tillsammans med luftens fuktighet ger svavelsyrlighet ochsvavelsyra. • Detta orsakar en försurning av nederbörden, vilket i sin tur får till följd att mark och sjöar mer och mer försuras. • Den sura nederbörden också vittrar sönder byggnader. Det bildas också giftiga ämnen och tungmetaller i marken som följer med vatten in i växterna och skadar växterna.