Ele k tronegati flik , χ
150 likes | 320 Vues
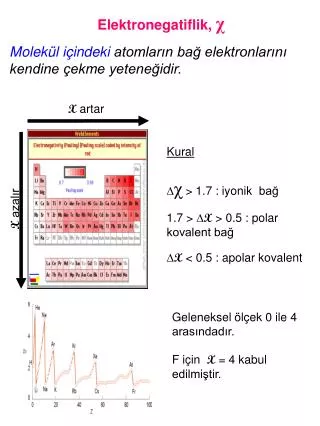
X artar. X azalır. Ele k tronegati flik , χ Molekül içindeki atomların bağ elektronlarını kendine çekme yeteneğidir. Kural D χ > 1.7 : i y oni k bağ 1.7 > D X > 0.5 : polar kovalent bağ D X < 0.5 : apolar k ovalent. Geleneksel ölçek 0 ile 4 arasındadır.

Ele k tronegati flik , χ
E N D
Presentation Transcript
Xartar Xazalır Elektronegatiflik, χ Molekül içindeki atomların bağ elektronlarını kendine çekme yeteneğidir. Kural Dχ > 1.7: iyonik bağ 1.7 > DX > 0.5 : polar kovalent bağ DX < 0.5 : apolar kovalent Geleneksel ölçek 0 ile 4 arasındadır. F için X= 4 kabul edilmiştir.
Bağ Polarlığı • Bağların polarlığı, bağ elektronlarının eşit olarak paylaşılmamasından kaynaklanır. • Bütün farklı atomlu bağlar, bir miktar polariteye sahiptir.
Hangi bağ daha polardır? O—FO—H 3.5 - 4.03.5 - 2.1 0.51.4 OH bağı, OF den daha polardır ve polaritesi ters yönlüdür.
Molekül Polaritesi Apolar Polar
DENEYSEL BİR ÖLÇÜM; DİPOL MOMENT Dipol Moment, = Qd Q = Yük d= Yüklü tanecikler arası uzaklık Birimi Debye(D) dir.
DİPOL MOMENTİN ÖLÇÜMÜ Metal plakalar arasında voltaj uygulanmamışken d- d+
DİPOL MOMENTİN ÖLÇÜMÜ - + Metal plakalar üzerine voltaj uygulandığında d- d+
Polar kovalent:Elektronlar eşit olmayan şekilde paylaşılır İyonik Bağ: Elektron alışverişi Apolar kovalentbağ:Elektronlar eşit bir şekilde paylaşılmış
Atomlar arasındaki elektronegativite farkı 0 ise, bağ apolar kovalenttir. Atomlar arasındaki elektronegativite farkı 0 ile 2.0 arasında ise, bağ polar kovalenttir, Atomlar elektronegativite arasındaki farkı 2.0 den büyük ise,bağ iyoniktir.
Dipol moment ve molekül yapısı Bazı durumlarda molekül içindeki bağlar polar olmakla beraber molekül apolar özellik gösterebilir. Molekülün polar veya apolar olması yük dağılımına göre açıklanır. - Molekülün şekli - Bağların polaritesi Polar Molekül (dipol) Moleküldeki artı yük merkezi ile eksi yük merkezi dengede değildir. Bir tarafı eksi diğer tarafı artı yük özelliği gösteriri Apolar molekül Molekülün uçlarında yük taşımayan Vaya uç kısımlarında aynı işaretli yük olan moleküller soru CH4, CH3Cl moleküllerinin polaritelerini açıklayınız