John Hunter 1794
It becomes our duty to adopt some artificial mode of conveying food intake into the stomach, by which the patient may be kept alive.

John Hunter 1794
E N D
Presentation Transcript
It becomes our duty to adopt some artificial mode of conveying food intake into the stomach, by which the patient may be kept alive. This was obtained by introduction of a very ingenious tube consisting of an eelskin, drawn over a flexible whalebone, fixed into a bladder containing the nutrients and medicines. The patient was given eggs beat up with little water, sugar and milk or wine. John Hunter 1794
Hvorfor er det på dag 3, at der skal tages stilling til ændring i planen?
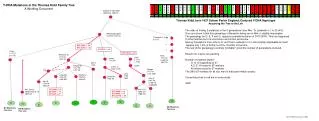
When to reach target? Based on Kondrup et al. Clin Nutr 2003; 22: 321-336
Recommendation: Based on 14 level 2 studies, we recommend early enteral nutrition (within 24-48 hours following admission to ICU) in critically ill patients. www.criticalcarenutrition.com
3 days’ Postoperative Feeding via Jejunal TubeInitiated 4 h after surgery (colectomy). 2N = 60. 30 days’ follow-up.Beier-Holgersen et al. Gut 1996;39:833-835
TEN complications Stratton RJ, Green CJ, Elia M. Disease-related malnutrition: an evidence-based approach.CABI Publishing 2003; p. 238
TEN mortality Stratton RJ, Green CJ, Elia M. Disease-related malnutrition: an evidence-based approach.CABI Publishing 2003; p 263
Effect of tube feeding on functional/clinical outcome Stratton RJ, Green CJ, Elia M. Disease-related malnutrition 2003; P. 260 & 263
Enteral better than parenteral • Reduced translocation: • increased IgA production (rats) • increased mucine production (rats) • increased mucosa thickness (rats) • Increased bactericidal function (rats) • Reduced cytokine production (humans) • Acquired immunization disappears with TPN (rats)
Arnt Ilve 03-07-2012Region HovedstadenEnhed for PatientsikkerhedHvidovre HospitalAnvendt filter: UTH Sonde.Der er anvendt følgende kriterier:Hændelsesbeskrivelse Indeholder "ernæring" ELLER Hændelsesbeskrivelse Indeholder "Sonde" sept 2005 - marts 2012: 118 hændelser; heraf 10 dødsfald (heraf 1 som ikke fik sondeernæring). Dvs 9 døde/79 mdr eller 1,4/år.Der anvendes ca. 11.000 sonder årligt i RegionH
Anlæggelse af nasogastrisk sonde • Ordination af behandling med fødesonde, hvilken kontrolprocedure der anvendes ved anlæggelsen og den senere daglige kontrol skal journalføres. • Anlæggelse foretages iført engangshandsker • Med patienten siddende i opret stilling udmåles med sonden afstanden fra toppen af epigastriet til bag øret, og herfra frem til næsetippen. Det bemærkes, hvilket mærke på sonden, der er ud for næsetippen • Sondespidsen påføres lokalbedøvende salve • Med patientens næse rettet lidt opad føres sonden langs bunden af næsehulen ned til svælget, indtil svælgrefleks kan mærkes • Herefter bøjer patienten hovedet længst muligt fremad og nedad. Med en smule vand, evt. via sugerør, stimuleres synkerefleksen, og samtidigt føres sonden ned i øsofagus, idet der skubbes på sonden, hver gang patienten synker. Man skal kunne mærke et let træk i sonden under synkebevægelserne. • Dette gentages et par gange, indtil det angivne mærke er ud for næsetippen. Guidewiren fjernes. RegionH vejledning 2010
Sundhedsstyrelsens”Vejledning om anvendelse af perorale fødesonder”(20. november 2002) • Den valgte kontrolprocedure for beliggenhed skal fremgå af afdelingens instruks. • Afdelingsledelsen har ansvaret for, at der foreligger en skriftlig instruks for kontrolprocedurer ved nedlæggelse, anvendelse og den daglige kontrol af fødesonder, samt at sundhedspersoner, til hvem sondenedlægning delegeres, har den fornødne kompetence. • Ordination af behandling med fødesonde, hvilken kontrolprocedure der skal anvendes ved anlæggelsen og den senere daglige kontrol skal journalføres • Den ordinerende læge skal tage stilling til hvilken kontrolprocedure, der skal anvendes i stedet for røntgenkontrol, både ved anlæggelse af sonden og ved de daglige kontroller
Kontrol af beliggenhedUmiddelbart efter anlæggelsen og før sonden anvendes • Den mest sikre metode er røntgenkontrol med indgift af kontrast i sonden. • Røntgenkontrol er uhensigtsmæssig i en række tilfælde (fx vågne og koopererende patienter med bevaret hoste- og synkerefleks og patienter, som af forskellige årsager skal have sonden genanlagt så hyppigt, at den samlede stråledosis bliver for stor, eller hvis røntgenkontrol ikke er tilgængelig). • Hos vågne patienter med bevarede hoste-/synkereflekser og en Ch 8 sonde udføres kontrol ved indblæsning af 10 ml luft i en sprøjte og samtidig stetoskopi af øvre abdomen (epigastriet/øvre ve. kvadrant). RegionH vejledning 2010
Kontrol af beliggenhed forts.Umiddelbart efter anlæggelsen og før sonden anvendes • Hos patienter med svækket bevidsthed eller svækkede hoste-/synkereflekser og en Ch 12 sonde udføres kontrol ved indblæsning af luft og desuden ved aspiration af ventrikelindhold, evt. aspiration af 10-15 ml indgivet væske. I tvivlstilfælde udføres røntgenkontrol. • Det skal angives i journalen, hvordan beliggenheden er kontrolleret. RegionH vejledning 2010
Efterfølgende daglig kontrol • Sonden kan displaceres fra den oprindelige placering, f.eks. ved opkastning, hoste eller ved at patienten ved et uheld har rykket i sonden, • Inden hver anvendelse af sonden skal beliggenheden igen kontrolleres. • Hos vågne patienter med bevarede hoste-/synkereflekser og en Ch 8 sonde: kontrol ved indblæsning af luft og samtidig stetoskopi af øvre abdomen (epigastriet). • Hos patienter med svækket bevidsthed eller svækkede hoste-/synkereflekser og en Ch 12 sonde: kontrol ved indblæsning af luft og desuden ved aspiration af ventrikelindhold, evt. aspiration af 10-15 ml indgivet væske. • Ved bolusindgift kontrolleres før hver bolus. • Ved kontinuerlig indgift kontrolleres før hver dags start og x 1 i hver efterfølgende vagt, hvor der gives sondeernæring. RegionH vejledning 2010
Indgift af sondeernæring • Sædvanligvis startes med kontinuerlig indgift, som medfører mindre risiko for diarré end bolusindgift. • Kontinuerlig indgift kan ske med eller uden pumpe. • Pt´s hovedgærde skal være eleveret til 30-45º under indgift af sondeernæring og indtil 2 timer efter mhp. at reducere risiko for aspiration til lungerne. • Sondeernæring kan gives i nattetimerne hos patienter, som er vågne og koopererende om dagen. • En pause på 4 timer f.eks. fra kl. 02-06 vil tillade ventriklens pH at falde til et baktericidt niveau, hvilket kan bidrage til at forebygge infektioner. Dette hensyn må vejes i forhold til behovet for adækvat ernæring. RegionH vejledning 2010
Indgift af sondeernæring forts • Dag 1 gives 500 ml i løbet af 10 timer, dvs. 50 ml/time sv.t. ca. 15 dråber pr. min. • Dag 2 gives 1000 ml i løbet af 15-20 timer, dvs. 50-65 ml/time sv.t. ca. 15-20 dråber pr. min. • Dag 3 gives 1500 ml i løbet af 15 -20 timer, dvs. 75-100 ml/time sv.t. ca. 25-30 dråber pr. min. • Dag 4 kan patientens individuelle behov gives med 100 ml pr. time, sv.t. ca. 30 dråber pr. min. RegionH vejledning 2010
Diaré Check: sondens placering bolus/kontinuerlig hastighed medicin (antibiotika) infektion præparat Behandling: mixt. codeinfosfat 8 mg/ml 10 ml x 2-4 (3 mg/ml indeholder sorbitol) mixt. imodium 0.2 mg/ml 10-20 ml x 2-4
TPN metaanalysis Koretz et al. Gastroenterology 2001; 121:970-1001.
Indikationer for TPN Koretz et al. Gastroenterology 2001; 121:970-1001.
Log regression n.s: energy and protein intake, size of study, publication year, diagnostic groups Kondrup et al. Clin Nutr 2003; 22: 321-336
TPN komplikationer • Mekaniske • Pnemothorax • Fejlplacering • Hydrothorax • Infektioner • Lokale • Systemiske (sepsis) • Venøs thrombose • Metaboliske • Hypoglyklæmi • Hyperglykæmi • Elektrolytforstyrrelser (Na+, K+, fosfat, magnesium) • Hypertriglyceridæmi --------- Langvarig (uger/måneder) ---------- • Leverpåvirkning • EFA mangel • Mangel på sporstoffer (Zn, Cu, Se) • Osteoporose Maroulis et al. Clin Nutr 2000; 19::295-304.
Monitorering Effekt Klinisk effekt Vægt Indtag dette Bivirkninger Væske/Na+ P-elektrolytter (fosfat, magnesium, kalium) Sonde PN
Refeeding syndrome:insulin-induced cellular uptake and redistribution of electrolytes in malnourished patients undergoing refeeding - a potentially lethal condition.