الفصل 3 خصائص الأحماض والقواعد
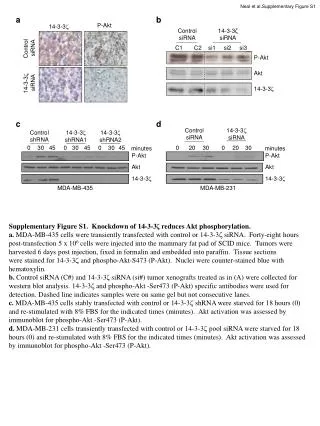
الفصل 3 خصائص الأحماض والقواعد. ا لصف ال ثاني عشر العلمي. القسم (1-3). خصائص الأحماض والقواعد. خصائص الأحماض والقواعد. أحماض شائعة في الغذاء :. * حمض اللاكتيك في اللبن. * حمض الأسيتيك في الخل. * حمض السيتريك في الحمضيات. * حمض الطرطريك في العنب. * حمض الفوسفوريك في المشروبات الغازية.

الفصل 3 خصائص الأحماض والقواعد
E N D
Presentation Transcript
الفصل 3خصائص الأحماض والقواعد الصف الثاني عشر العلمي
القسم (1-3) خصائص الأحماض والقواعد
خصائص الأحماض والقواعد أحماض شائعة في الغذاء : * حمض اللاكتيك في اللبن * حمض الأسيتيك في الخل . * حمض السيتريك في الحمضيات . * حمض الطرطريك في العنب . * حمض الفوسفوريك في المشروبات الغازية .
قواعد شائعة الاستعمال : * الأمونيا في عمليات التنظيف العامة . * هيدروكسيد الصوديوم مكون المنظفات . * حليب الماغنيسيا مضاد للحموضة . * هيدروكسيد الألومنيوم مضاد للحموضة . * كربونات الصوديوم الهيدروجينية مضاد للحموضة .
خصائص الأحماض * مذاق محاليلها المائية حامض . * تغير ألوان الكواشف . * بعضها يتفاعل مع الفلزات النشيطة وينطلق غاز الهيدروجين . * تتفاعل مع القواعد معطية ملحاً وماء * محاليلها المائية موصلة للكهرباء .
تسمية الأحماض تعريف الحمض الثنائي : حمض يحتوي على عنصرين فقط هما الهيدروجين وعنصر آخر أكثر سالبية كهربائية . أمثلة : * كثير من الأحماض غير العضوية الشائعة :HI , HBr , HCl , HF
تسمية الأحماض الثنائية : (هيدرو ) 1- يبدأ بالبادئة جذر اسم العنصر الثاني 2- يتبع (يك ) 3- ينتهي باللاحقة
H F (هيدرو ) هيدرو 1- يبدأ بالبادئة جذر اسم العنصر الثاني 2- يتبع فلور (يك ) يك 3- ينتهي باللاحقة
اسم الحمض الصيغة يك فلور هيدرو HF يك كلور هيدرو HCl يك برومـ هيدرو HBr يك يود هيدرو HI
تعريف الحمض الأكسجيني : حمض يتكون من الهيدروجين والأكسجين وعنصر ثالث لافلزي في الغالب .
اسم الحمض اسم الآنيون الصيغة نيتريت NO2- النيتروز HNO2 نيترات NO3- النيتريك HNO3 الفوسفوروز H3PO3 فوسفيت PO33- فوسفات H3PO4 PO4- الفوسفوريك الكبريتوز H2SO3 كبريتيت SO32- الكبريتيك H2SO4 كبريتات SO42-
اسم الحمض اسم الآنيون الصيغة HClO هيبوكلوريت CIO- هيبوكلوروز كلوريت CIO2- كلوروز HClO2 كلورات CIO3- كلوريك HClO3 بيركلورات CIO4- بيركلوريك HClO4 اليوديك HIO3 يودات IO3-
بعض الأحماض الصناعية الشائعة حمض الكبريتيك : حمض النيتريك : حمض الفوسفوريك : حمض الهيدروكلوريك : حمض الأسيتيك :
الـقــواعـد * مذاق محاليلها المائية مر . * تغير محاليلها ألوان الكواشف . * محاليلها المائية المخففة ذات ملمس صابوني . *تتفاعل مع الأحماض وينتج ملح وماء تختفي خصائص القاعدة عند إضافة كمية مكافئة من الحمض . * محاليلها المائية موصلة للكهرباء .
أحماض وقواعد أرهينيوس حمض أرهينيوس: مركب كيميائي يزيد من تركيز أيون الهيدروجين H+ في المحلول المائي. قاعدة أرهينيوس: مركب كيميائي يزيد من تركيز أيون الهيدروكسيد OH- في المحلول المائي.
المحاليل المائية للأحماض أحماض أرهينيوس: مركبات جزيئية تحتوي على ذرات الهيدروجين القابلة للتأين . تفاعل حمض النيتريك مع الماء : HNO3 + H2O H3O+ + NO3-
- + + ماء حمض النيتريك H2O HNO3 + أيون النيترات أيون الهيدررونيوم H3O+ NO3-
تأين جزيئات كلوريد الهيدروجين في حمض الهيدروكلوريك : HCl + H2O H3O+ + Cl- جميع الأحماض القابلة للذوبان في الماء هي إلكتروليتات .
قوة الأحماض الحمض القوي : الحمض الذي يتأين بشكل تام في المحلول المائي . تعتمد قوة الحمض على : * قطبية الرابطة بين الهيدروجين والعنصر المرتبط به . * طاقة الرابطة .
ماذا يحتوي محلول الحمض القوي ؟ الأيونات فقط .( أيونات الهيدرونيوم وآنيونات ). ماذا يحتوي محلول حمض الهيدروكلوريك ؟ H3O+ Cl- HCl H2O + + أيونات الهيدرونيوم وآنيونات ). Cl-
الحمض الضعيف : الحمض الذي ينتج القليل من أيونات الهيدروجين في المحلول المائي . ماذا يحتوي محلول الحمض الضعيف ؟ الأيونات والجزيئات ( أيونات الهيدرونيوم وآنيونات وجزيئات ) .
ماذا يحتوي محلول حمض الهيدروسيانيك ؟ CN- HCN H2O + H3O+ + أيونات الهيدرونيوم وآنيونات وجزيئات CN- HCN
أحماض شائعة/ قوية H3O+ Cl- HCl H2O + + H3O+ ClO4- H2O HClO4 + + H3O+ Br- HBr H2O + + H3O+ l- Hl H2O + + H3O+ HSO4- H2O + H2SO4 + H3O+ ClO3- H2O HClO3 + +
أحماض شائعة/ ضعيفة SO42- H2O + HSO4- + H3O+ H2O H2PO4- H3PO4 + H3O+ + F- HF H2O + H3O+ + H2O CH3COOH + CH3COO- H3O+ +
تابع أحماض شائعة/ ضعيفة H3O+ HCO3- H2O + H2CO3 + H3O+ HS- H2O + H2S + CN- HCN H2O + H3O+ + H3O+ CO32- H2O + HCO3- +
المحاليل المائية للقواعد معظم القواعد مركبات أيونية تحتوي على كاتيون فلزي وآنيون الهيدروكسيدOH- H2O NaOH(S) Na+ OH- + H2O Ca(OH)2(S) Ca2+ 2 OH- +
القواعد ليست كلها مركبات أيونية، الأمونيا مركب جزيئي له خاصة قاعدية ، لماذا ؟ بسبب تكون آنيونات الهيدروكسيدOH- عند تفاعلها مع الماء .كما في المعادلة : NH3 + H2O OH- NH4+ +
قوة القواعد تعتمد قوة القواعد على : درجة تفككها ( مدى تزويدها للمحلول المائي بأيونات الهيدروكسيد ) . القواعد التي لا تذوب جيداً في الماء لا تنتج عدداً كبيراً من أيونات الهيدروكسيد فلا تكون محاليها قلوية قوية .
تعتمد قلوية المحاليل على : تركيز أيونات الهيدروكسيد فيها ، وليس على عدد أيونات الهيدروكسيد الموجودة في المركب الذائب . تعتبر الأمونيا إلكتروليتاً ضعيفاً (قاعدة ضعيفة) على الرغم أنها جيدة الذوبان في الماء ، لماذا؟ لأن تركيز أيونات الهيدروكسيد قليل في محلولها
قواعد قوية NaOH Na+ OH- + KOH K+ OH- + RbOH Rb+ OH- + CsOH Cs+ OH- +
تابع/ قواعد قوية H2O Ca(OH)2 Ca2+ 2 OH- + H2O Sr(OH)2 Sr2+ 2 OH- + H2O Ba(OH)2 Ba2+ 2 OH- +
قواعد ضعيفة NH3 + H2O OH- NH4+ + C6H5NH2 + H2O OH- C6H5NH3+ +
القسم (2-3) نظريات الأحماض - القواعد
القسم (2-3) نظريات الأحماض - القواعد
أحماض وقواعد برونشتيد – لوري أحماض برونشتيد – لوري : جزيء أو أيون مانح للبروتون . قواعد برونشتيد – لوري : جزيء أو أيون مستقبل للبروتون .
حسب برونشتيد – لوري : الحمض : يمنح ( يعطي ) بروتون H+. القاعدة : تستقبل ( تأخذ ) بروتون H+. NH3 HCl H Cl- + NH4+ + يمنح تستقبل قاعدة حمض
: : :Cl: :O: H H H + : : H قاعدة حمض تستقبل + يمنح : : - :O: H H :Cl: + : : H
H : : :Cl: :N: H H H + : : H حمض قاعدة + H : : - :N: H H :Cl: + : : H
الماء يتفاعل أيضاً كحمض برونشتيد– لوري : : :O: H :N: H H H + : : H H حمض قاعدة - + H : : :O: :N: H H + : H : H
الحمض أحادي البروتون : الحمض الذي يمنح بروتون واحداً ( أيون الهيدروجين ) فقط من كل جزيء . أمثلة : حمض الهيدروكلوريك HCl حمض النيتريك HNO3 حمض البيركلوريك HClO4
كيف يمنح جزيء من الحمض أحادي البروتون HClبروتوناً لجزيء الماء ؟ يتأين الحمض HCl بخطوة واحدة ليكون Cl- و H3O+ H2O HCl H3O+ Cl- + +
الحمض متعدد البروتون : الحمض الذي يمنح أكثر من بروتون من كل جزيء . أمثلة : حمض الكبريتيك H2SO4 حمض الفوسفوريك H3PO4
تتأين الأحماض المتعددة البروتون في أكثر من خطوة ( مراحل متعددة ) حيث يفقد في كل مرحلة أيوناً من الهيدروجين .
يتأين حمض الكبريتيك على مرحلتين : المرحلة الأولى :- حمض الكبريتيك قوي يتحول بشكل تام إلى أيونات الكبريتات الهيدروجينية: H3O+ HSO4- H2O + H2SO4 + المرحلة الثانية :- أيون الكبريتات الهيدروجينيةحمض ضعيف يتأين (حالة اتزان ) كما يلي : HSO4- H2O + H3O+ + SO42-
ماذا يحتوي محلولحمض الكبريتيك ؟ H3O+ HSO4- أيونات SO42- كم بروتونا يمنح جزيء حمض الكبريتيك ؟ 2 بروتون لذلك فهو حمض ثنائي البروتون وبالتالي فهو من الأحماض البروتون متعددة
الحمض ثنائي البروتون : هو الذي يمنح بروتونين اثنين من كل جزيء . حمض الفوسفوريك من الأحماض متعددة البروتون فهو حمض ثلاثي البروتون . الحمض ثلاثي البروتون : هو الذي يمنح ثلاثة بروتونات من كل جزيء .
H2O H2PO4- H3PO4 + H3O+ + H2PO4- H2O + H3O+ + HPO42- HPO42- H2O + H3O+ + PO43- ماذا يحتوي محلولحمض الفوسفوريك ؟ H3PO4 PO43- HPO42- H2PO4- H3O+
في معظم الأحماض متعددة البروتون : يكون تركيز الأيونات المتكونة في المرحلة الأولى هو الأكبر . وينخفض بحسب مراحل التأين . ففي محلولحمض الفوسفوريك يكون تركيز H2PO4- > HPO42- > PO43- لذلك يعد حمض الفوسفوريكضعيفاً في كل مرحلة تأين له .
أحماض وقواعد لويس حمض لويس : ذرة أو جزيء أو أيون يستقبل زوجاًمن الإلكتروناتليكون رابطة تساهمية. قاعدةلويس : ذرة أو جزيء أو أيون يمنح زوجاًمن الإلكتروناتليكون رابطة تساهمية.
قواعد لويس H . . :N. H . . . H N تحتوي على 7 إلكترونات ترتيبه (2 ,5) بينما ذرةH تحتوي على 1. زوج إلكترونات غير مشارك في رابطة يمكن منحه