CROMATOGRAFIA GASOSA
831 likes | 1.63k Vues
CROMATOGRAFIA GASOSA. Introdução . CLASSIFICAÇÃO DOS MÉTODOS INSTRUMENTAIS. - Colorimetria Espectrofotometria no visível e ultravioleta Espectrofotometria no infravermelho - Espectrofluorimetria Espectroscopia de absorção atômica Espectroscopia de emissão atômica.

CROMATOGRAFIA GASOSA
E N D
Presentation Transcript
CROMATOGRAFIAGASOSA Profa. Denise Moritz
Introdução CLASSIFICAÇÃO DOS MÉTODOS INSTRUMENTAIS • - Colorimetria • Espectrofotometria no visível e ultravioleta • Espectrofotometria no infravermelho • - Espectrofluorimetria • Espectroscopia de absorção atômica • Espectroscopia de emissão atômica Espectroanalíticos - Cromatografia Líquida - Cromatografia Gasosa Cromatográficos • - Eletrogravimetria • Amperometria • Condutimetria • - Coulometria • - Potenciometria • - Voltametria • - Polarografia Eletroanalíticos
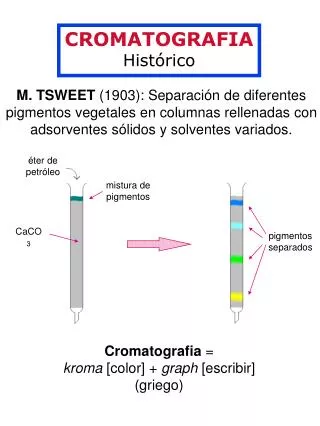
éter de petróleo mistura de pigmentos CaCO3 pigmentos separados Introdução HISTÓRICO M. TSWEET (1903): Separação de misturas de pigmentos vegetais em colunas recheadas com adsorventes sólidos e solventes variados. Cromatografia = kroma [cor] + graph [escrever] (grego) Profa. Denise Moritz
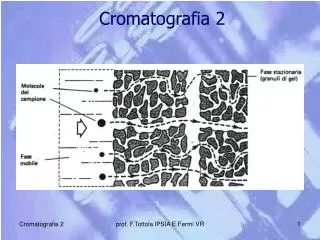
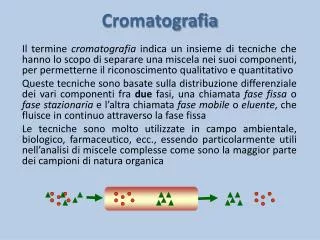
A cromatografia envolve uma série de processos de separação de misturas, acontece pela passagem de uma mistura através de duas fases: uma estacionária (fixa) e outra móvel. A interação dos componentes da mistura com estas duas fases é influenciado por diferentes forças intermoleculares, incluindo iônica, bipolar, apolar, e específicos efeitos de afinidade e solubilidade. Introdução Profa. Denise Moritz
1940 1950 1960 Histórico “CGS” rudimentar CGL proposta (Martin e Synge) Separação de ácidos orgânicos por CGL: primeiro cromatógrafo (Martin e James) Primeiro equipamento comercial (Griffin & George) Detector por Densidade de Gás (Martin e James) Detector por Ionização em Chama (McWillian e Dewar) Detector por Captura de Eletrons (Lovelock e Lipsky) Colunas Capilares (Golay) Presentemente: Vendas de equipamentos e acessórios para CG nos EUA estimadas em mais de US$ 750.000.000 (1995). Profa. Denise Moritz
Introdução INSTRUMENTOS PARA ANÁLISE Informação interpretada pelo homem características físicas e químicas do analito Instrumento Informação armazenada Estímulo Resposta Fonte de energia Sistema em estudo Informação analítica
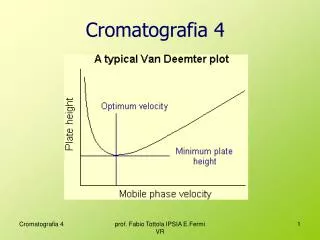
Introdução Tempo de retenção - tempo quedecorredesde a injecçãoatémeiaeluição; Tempo morto; - (tm) =tempo necessáriopara um produto “nãoretido” atravessar a coluna Vazão volumétrica; Fase móvel (eluente); Fase Estacionária (fase fixa – ex.Coluna) Seletividade da coluna; Eficiência da coluna – número de pratos; Número de separação; Tempo de análise. Profa. Denise Moritz
tR = Tempo de Retenção (tempo decorrido entre a in-jeção e o ápice do pico cromatográfico) Introdução Tempo de Retenção Ajustado, tR‘ O parâmetro diretamente mensurável de retenção de um analito é o TEMPO DE RETENÇÃO AJUSTADO, tR’: SINAL TEMPO Profa. Denise Moritz
Introdução CONCEITOS • Tempo de retenção: • É o tempo que a amostralevaparapercorrer a coluna (éretida do sistema) • Oscomponentes da amostrasãocomparados com o de padrõesanteriorestestadosno aparelho.file://localhost/Users/Denise/Análise Instrumental Unisul/slide 3.ppt Profa. Denise Moritz
COLLEGE OF CHARLESTON DEPARTMENT OF CHEMISTRY AND BIOCHEMISTRY. Determination of methyl salicylate in rubbing alcohol by gas chromatography using the method oh standard addtionsDisponívelem:<http://kinardf.people.cofc.edu/221LabCHEM/CHEM221L%20Gas%20Chromatography%20of%20Methyl%20Salicylate.htm>. Data de acesso; 24/04/2011 Profa. Denise Moritz
ÁREA Profa. Denise Moritz
A cromatografia pode ser utilizada para a- identificação de compostos, por comparação com padrões previamente existentes, - para a purificação de compostos, separando-se as substâncias indesejáveis e para a separação dos componentes de uma mistura. Introdução Profa. Denise Moritz
Aplicabilidade Quais misturas podem ser separadas por CG ? (para uma substãncia qualquer poder ser “arrastada” por um fluxo de um gás ela deve ser dissolver - pelo menos parcialmente -nesse gás) Misturas cujos constituintes sejam VOLÁTEIS (=“evaporáveis”) DE FORMA GERAL: CG é aplicável para separação e análisede misturas cujos constituintes tenham PONTOS DE EBULIÇÃO de até 300oCe que termicamente estáveis. Profa. Denise Moritz
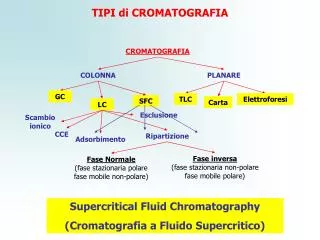
As diferentes formas de cromatografia podem ser classificadas considerando-se diversos critérios:1. Classificação pela forma física do sistema cromatográfico2. Classificação pela fase móvel empregada3. Classificação pela fase estacionária utilizada4. Classificação pelo modo de separação Classificação Profa. Denise Moritz
Modalidades e Classificação Cromatografia Líquida FM = Líquido Cromatografia Gasosa (CG) FM = Gás Cromatografia Gás-Sólido (CGS) Sólida Em CG a FE pode ser: Cromatografia Gás-Líquido (CGL) Líquida Profa. Denise Moritz
Em relação à forma física do sistema,a cromatografia pode ser subdividida em cromatografia em coluna e cromatografia planar. EM COLUNA: cromatografia líquida, gasosa e supercrítica. PLANAR: Centrífuga, em papel e camada delgada. Classificaçãopela forma física do Sistemacromatográfico Profa. Denise Moritz
São de 3 tipos: cromatografia gasosa, cromatografia líquida e a cromatografia supercrítica (CSC). A cromatografia líquida apresenta uma importante subdivisão: a cromatografia líquida clássica (CLC) e a cromatografia líquida de alta eficiência (CLAE). No caso de fases móveis gasosas, separações podem ser obtidas por cromatografia gasosa (CG) e por cromatografia gasosa de alta resolução (CGAR). Classificação pela fase móvel empregada Profa. Denise Moritz
COLUNAS CROMATOGRÁFICAS Profa. Denise Moritz
Quanto à fase estacionária, distingue- se entre fases estacionárias sólidas, líquidas e quimicamente ligadas. No caso da fase estacionária ser constituída por um líquido, este pode estar simplesmente adsorvido sobre um suporte sólido ou imobilizado sobre ele. Suportes modificados são considerados separadamente, como fases quimicamente ligadas, por normalmente diferirem dos outros dois em seus mecanismos de separação. Classificação pela fase estacionária empregada Profa. Denise Moritz
Colunas cromatográficas • Empacotadas: • Fabricadas depositando-se um filme da fase estacionária líquida sobre um material inerte chamado suporte. • De comprimento e diâmetro otimizados p/ análise da amostra de interesse. • Capilares: • Fabricadas depositando um filme finíssimo de 0,1 e 5 microns na fase estacionária nas paredes de um tubo capilar. • Tubos: aço inoxidável, vidro, níquel e sílica gel. • Muito mais eficientes. Profa. Denise Moritz
Princípio Básico Separação de misturas por interação diferencial dos seus componentes entre uma FASE ESTACIONÁRIA (líquido ou sólido) e uma FASE MÓVEL (líquido ou gás). Profa. Denise Moritz
Parafinas – apolares Poliglicóis – polares Poliésteres - polares Silicones – cobrem ampla faixa de polaridade. Fases estacionárias utilizadas Profa. Denise Moritz
Colunas Cromatográficas • Contém fase estacionária; • Metal, vidro, sílica fundida; • Colunas empacotadas; • Colunas micro-empacotadas; • Colunas capilares; • Seletividade e eficiência. COLUNA Amostras Líquidas Amostras Gasosas empacotada 0,2 L ... 20 L 0,1 ml ... 50 mL capilar 0,01 L ... 3 L 0,001 ml ... 0,1 mL Profa. Denise Moritz
Colunas Empacotadas • Diâmetros: 2, 3 ou 4mm; • Comprimento: 0,5m - 5m; • O suporte não polar deve ser totalmente desativado se for analisar compostos polares. EMPACOTADA L = 0,5 m a 5 m Profa. Denise Moritz
ColunasCapilares • Flexíveis; • Mecanicamente duráveis; • Quimicamente inertes; • Diâmetro interno de 0,25 – 0,32 mm/ L= 5m – 100m; • Picos mais finos = melhor separação; • Aumenta a velocidade de análise; • Mais de 100.000 pratos; • Melhor forma de pico, melhor estabilidade da coluna; • Bom para separar misturas com muitos componentes. CAPILAR L = 5 m a 100 m Profa. Denise Moritz
Características das Colunas Profa. Denise Moritz
FE líquida SUPORTE Sólido inerte poroso Tubo capilar de material inerte Entrecruzada: as cadeias poliméricas são quimicamente ligadas entre si Quimicamente ligadas: as cadeias poliméricas são “presas” ao suporte por ligações químicas Colunas LÍQUIDOSDepositados sobre a superfície de: sólidos porosos inertes (colunas empacotadas) ou de tubos finos de materiais inertes (colunas capilares) Para minimizar a perda de FE líquida por volatilização, normalmente ela é: SÓLIDOSColunas recheadas com material finamente granulado (empacotadas) ou depositado sobre a superfície interna do tubo (capilar) Profa. Denise Moritz
1 6 2 4 5 3 O Cromatógrafo a Gás 1 - Reservatório de Gás e Controles de Vazão / Pressão. 2 - Injetor (Vaporizador) de Amostra. 3 - Coluna Cromatográfica e Forno da Coluna. 4 - Detector. 5 - Eletrônica de Tratamento (Amplificação) de Sinal. 6 - Registro de Sinal (Registrador ou Computador). Observação: em vermelho: temperatura controlada Profa. Denise Moritz
Colunas CROMATOGRAFIA A distribuição de um soluto entre a parte móvel e a estacionária pode envolver fenômenos de : • Partição, • Adsorção • Exclusão e troca iônica Técnica de fracionamento Em diferentes velocidades com que cada uma se move através de uma fase estacionária (porosa) ao serem arrastadas por uma fase móvel. Profa. Denise Moritz
CROMATOGRAFIA GASOSA • Utilizada na separação e identificação de substâncias: • Que possam ser volatilizadas sem sofrer decomposição; • Não voláteis que possam ser convertidas em derivados voláteis. • A fase móvel é um gás que percola a coluna. Profa. Denise Moritz
Técnica de: Alta eficiência Efetuada num tempo razoável Utilizando mínimas quantidades. Profa. Denise Moritz
SELETIVADeve interagir diferencialmente com os componentes da amostra. FE Seletiva: separação adequada dos constituintes da amostra FE pouco Seletiva: má resolução mesmo com coluna de boa eficiência Características de uma FE ideal Regra geral: a FE deve ter características tanto quanto possível próximas das dos solutos a serem separados (polar, apolar, aromático ...) Profa. Denise Moritz
AMPLA FAIXA DE TEMPERATURAS DE USOMaior flexibilidade na otimização da separação. BOA ESTABILIDADE QUÍMICA E TÉRMICAMaior durabilidade da coluna, não reage com componentes da amostra POUCO VISCOSAColunas mais eficientes (menor resistência à transferência do analito entre fases) DISPONÍVEL EM ELEVADO GRAU DE PUREZAColunas reprodutíveis; ausência de picos “fantasma” nos cromatogramas. FASES ESTACIONÁRIAS Características de uma FE ideal Profa. Denise Moritz
Sólidos com grandes áreas superficiais (partículas finas, poros) Solutos polares ADSORÇÃO Sólidos com grande número de sítios ativos (hidroxilas, pares de eletrons...) Características de uma FE ideal Fase Estacionária SÓLIDA - O fenômemo físico-químico responsável pela interação analito + FE sólida é aADSORÇÃO A adsorção ocorre na interface entre o gás de arraste e a FE sólida Profa. Denise Moritz
- Sólidos finamente granulados (diâmetros de partículas típicos de 105 µm a 420 µm). - Grandes áreas superficiais (até 102 m2/g). - Separação de gases fixos - Compostos leves - Séries homólogas Principais Aplicações: EXEMPLOS - FE ideal Características Gerais: Mais usados: Polímeros Porosos Porapak (copolímero estireno-divi-nilbenzeno), Tenax (polióxido de difenileno) Sólidos Inorgânicos Carboplot, Carboxen (carvões ativos grafitizados), Alumina, Peneira Molecular (argila microporosa) GASES DE REFINARIA Coluna:Carboxen-1000 60-80 mesh; 15’ x 1/8” TCOL: 35oC a 225oC / 20oC. min-1 Gás de Arraste: He @ 30 ml.min-1 Detector: TCD Profa. Denise Moritz
POLIGLICÓISMuito polares; sensíveis a umidade e oxidação; ainda muito importantes. Principal: Polietilenoglicol (nomes comerciais: Carbowax, DB-Wax, Supelcowax, HP-Wax, etc.) Estrutura Química: Exemplos - FASES ESTACIONÁRIAS Famílias de FE Líquidas AMINAS ALIFÁTICAS Coluna:4 % Carbowax 20M s/ Carbopack B + 0,8% KOH TCOL: 200oC (isotérmico) Gás de Arraste: N2 @ 20 mL.min-1 Detector: FID Amostra: 0,01 mL da mistura de aminas Profa. Denise Moritz
FaseMóvel Profa. Denise Moritz
EXEMPLOS DE FASES MÓVEIS Pressurizados em torpedos de aço c/ pressão aproximada entre 120 e 200 atm. Fluxo Coluna: 0,5 – 80 mL/min GÁS DE ARRASTE: Hidrogênio Nitrogênio Argônio Hélio Profa. Denise Moritz
Detectores Profa. Denise Moritz
Detector Dispositivo que transforma um sinal elétrico conveniente a variação da composição do gás de arraste ao sair da coluna cromatográfica. O sinal é registrado e a área dos picos, integrada para fins de quantificação. Existem em torno de 20 tipos, porém apenas 5 ou 6 tem aplicação em grande quantidade. Profa. Denise Moritz
Osprincipaisdetectoressão: Condutividadetérmica – DCT Captura de elétrons – DCE Fotômetro de chama DFC Termoiônico - DFC Ionização de chama – DIC Profa. Denise Moritz
DIC ou FID O gás de arraste proveniente da coluna (N2) é queimado em presença de ar e H2. A chama produzida encontra-se num campo elétrico. Durante a combustão de compostos orgânicos contendo H2 há formação de radicais livres – ionizados pelo campo elétrico – formando sinais – amplificados produzindo picos. Profa. Denise Moritz
Detectores Dispositivos que examinam continuamente o material eluido, gerando sinal quando da pas-sagem de substâncias que não o gás de arraste Gráfico Sinal x Tempo = CROMATOGRAMA Idealmente: cada substância separada aparece como um PICO no cromatograma. Profa. Denise Moritz
DETECTOR POR CONDUTIVIDADE TÉRMICA (DCT OU TCD)Variação da condutividade térmica do gás de arraste. DETECTOR POR IONIZAÇÃO EM CHAMA (DIC OU FID)Íons gerados durante a queima dos eluatos em uma chama de H2 + ar. DETECTOR POR CAPTURA DE ELÉTRONS (DCE OU ECD)Supressão de corrente causada pela absorção de elétrons por eluatos altamente eletrofílicos. ANALÓGICO Registradores XY REGISTRO DE SINAL DIGITAL Integradores Computadores Detectores – Mais comuns Profa. Denise Moritz
INJETOR / INJEÇÃO Profa. Denise Moritz
INJETOR / INJEÇÃO Profa. Denise Moritz
PROCESSO CROMATOGRÁFICO Introduz-se a fase estacionária num tubo A fase móvel é bombeada continuamente a uma velocidade constante e controlada. As substâncias começam a migrar de acordo c/ as interações de suas propriedades físico-químicas (c/ as da FM e FE) Passam por um detector no final da coluna, que são captados por um registrador. O sinal é proporcional à sua concentração. O gráfico Obtido - CROMATOGRAMA Profa. Denise Moritz