Q-Dots
Q-Dots. INTEGRANTES Figoli, Gustavo González Bardeci, Nicolas Nasi, Marcelo Santoro, Natalia Spedalieri, Cecilia Villa, Leticia. Introducción. Los nanomateriales presentan propiedades físicas y químicas muy diferentes a aquellas de su forma “bulk”.

Q-Dots
E N D
Presentation Transcript
Q-Dots INTEGRANTES Figoli, Gustavo González Bardeci, Nicolas Nasi, Marcelo Santoro, Natalia Spedalieri, Cecilia Villa, Leticia
Introducción • Los nanomateriales presentan propiedades físicas y químicas muy diferentes a aquellas de su forma “bulk”. • Las nanopartículas de materiales semiconductores, llamados puntos cuánticos o Q-Dots, presentan propiedades ópticas únicas, por lo que se les han encontrado numerosas aplicaciones. • Principalmente son dos los efectos observados (a nivel de la estructura electrónica) como consecuencia de la reducción progresiva del tamaño de partícula en la nanoescala .El incremento del Band gap y la discretización de los niveles de energía (es decir que no existe un continuo de estados accesibles, sino que el diagrama de niveles de energía se limita a una serie de niveles discretos que se asemejan más a la escala molecular que a la de un sólido extendido) • Una vez exitado, el electrón y el hueco pueden recombinarse. La recombinación radiativa puede dar lugar a una banda de emisión relativamente angosta (Eg) o a una banda de emisión relativamente más ancha centrada a energías menores. Esto es debido a la presencia de defectos de borde. Debido a la alta relación área / volumen, la presencia de defectos de borde es importante.
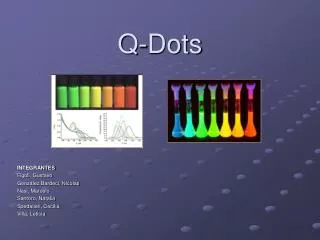
Introducción • Hay una relación entre el tamaño de partícula y los espectros de absorción y emisión, o sea que se puede controlar la longitud de onda de la luz que se emite, con el tamaño de los puntos cuánticos . • Debido a estas características y a su tamaño nanometrico se han hecho aplicaciones en teoria computacional, donde la luz es utilizada para procesar la información, los estados cuánticos de los electrones se pueden usar como bits (qbits) para codificar la información. • Se usan como sondas biológicas fluorescentes, debido a su fotoluminiscencia ajustable según tamaño de partícula, en lugar de células teñidas y a que emiten una intensidad mucho mayor. • Los puntos de Quantum incorporan los mejores aspectos de emisores orgánicos e inorgánicos, al servicio de los displays electroluminicentes. Leds Moléculas teñidas
Objetivo • Obtención de nanopartículas de ZnS, CdS y PbS, de diferentes tamaños de partícula. • Técnica: Micelas inversas.
Técnica experimental • Se disuelve el compuesto orgánico AOT que se usa como surfcactante, en ciclohexano; se agrega una cantidad variable de agua. Se forman asi micelas inversas cuyas cabezas polares quedan hacia adentro. El tamaño de la micela va a quedar limitado por la cantidad de agua agregada. • Luego se agregan las soluciones de sulfuro y de metal por separado, agitando para evitar precipitación del sulfuro metalico. • Como las nanopartículas se van a sintetizar en el interior de la micela, se puede controlar el tamaño de las mismas variando la relación w = H2O/AOT • A mayor W mayor tamaño de partícula. AOT bis(etil-2-hexil)sulfosuccinato Micela inversa
Caracterización Métodos Absorción UV-Visible Fluorescencia Absorción: Cuando se irradia el material con radiación electromagnética de energía superior a Eg, pueden promoverse electrones de la banda de valencia a la banda de conducción, formándose pares electrón – hueco por absorción de esa radiación. Existen modelos que relacionan la intensidad de la radiación absorbida con el tamaño de partícula. Típicamente se emplea la ecuación de Brus (Eq. 1), que se basa en un modelo de partícula en una caja esférica con una barrera de potencial infinita. La misma sólo es válida cuando existen efectos de confinamiento cuántico, cuando el radio ha descendido por debajo del radio de Bohr del excitón Utilizando esta ecuación puede calcularse la energía de la transición electrónica de menor energía, Eg donde eoo es la permitividad relativa del material, y m*e y m*h son las masas efectivas del electrón y el hueco, respectivamente.
Caracterización • Fotoluminiscencia El electrón y el hueco pueden recombinar de forma radiativa o no radiativa. La recombinación radiativa puede dar lugar a una banda de emisión relativamente angosta, centrada aproximadamente en Eg (banda de recombinación del excitón) y/o a una banda de emisión relativamente más ancha centrada a energías menores, debido a la presencia de defectos que se ven involucrados en el proceso de recombinación. Debido a la alta relación área / volumen, la presencia de defectos de borde es importante y suele primar el segundo mecanismo.
Resultados – Absorción UV El pico excitónico muestra la longitud de onda en la cual la muestra absorbe radiación, formando un par electrón-hueco (par excitónico) Para determinarlo, se registró en cada espectro la longitud de máxima absorción observada.
Resultados • Cálculo de Eg • Se puede estimar el valor de Eg para las nanopartículas preparadas. Esto se realizó tomando como Eg el valor del umbral de absorción (“band edge”) es decir, la energía a partir de la cual la muestra comienza a absorber. Este valor indica que esa es la longitud de onda mínima necesaria para excitar un electrón hacia niveles de energía superiores. En la práctica, esto se obtuvo gráficamente como la intersección entre la línea de base y la caída de la banda de absorción. Sin embargo este cálculo es sólo una aproximación, dado que la presencia de estados localizados a energías levemente mayores que la banda de valencia y a energías levemente menores que la banda de conducción permite transiciones a mayores longitudes de onda que la del band gap. A continuacion se muestran también los valores del radio de las partículas, calculados según la ecuación de Brus, tomando como Eg de las mismas los valores obtenidos por el método indicado anteriormente
Resultados - Fluorescencia Se midieron los espectros de fluorescencia para todos los sulfuros con sus distintos tamaño de particula. • CdS Espectro de excitación Espectro de emisión
Resultados - Fluorescencia ZnS PbS Los espectros (emisión y excitación) de los sulfuros de Pb y Zn están solapados con los del ciclohexano. Esto no ocurre para el sulfuro de cadmio. Esto puede deberse a que la intensidad de los espectros medidos para CdS es mucho mayor que aquella para los otros sulfuros.
Resultados - Comparación entre los metales a un mismo w W = 2 Se observa dependencia del límite de absorción con el metal, que se correlaciona a su vez con el Band Gap del material Bulk. λ intersección: ZnS < CdS < PbS
Resultados – Variación de [Cd2+] Se midieron los espectros de UV y fluorescencia para tres concentraciones diferentes de Cd2+. Se observa que no cambia λ en el espectro UV, pero ninguna tendencia se distingue.
Resultados – Otras Caracterizaciones Se usaron las técnicas de ME y ESA. En las micrografías se observaron agregados micelares que evitaron que veamos los qdots Los elementos hallados corresponden a los utilizados a lo largo de toda la síntesis de los q-dots.