La formation des ions
La formation des ions. Quels ions vont former les différents éléments chimiques ?. La formation des ions. Règles de l’octet (ou du duet):

La formation des ions
E N D
Presentation Transcript
La formation des ions Quels ions vont former les différents éléments chimiques ?
La formation des ions Règles de l’octet (ou du duet): Pour se stabiliser, les atomes de tous les éléments chimiques ont tendance à modifier leur structure électronique pour avoir une couche externe qui contient 2 électrons (couche K) ou 8 électrons (couches L, M,…). Application à la formation des ions : Un atome qui forme un ion perd ou gagne des électrons pour acquérir la structure électronique du gaz noble le plus proche de lui dans la classification périodique.
La formation des ions Exemple de la famille des alcalins: le sodium
Atome Na neutron (K)2(L)8(M)1 proton 1 e- externe électron La formation des ions Na Sodium Z = 11 Comment faire pour appliquer la règle de l’octet ???
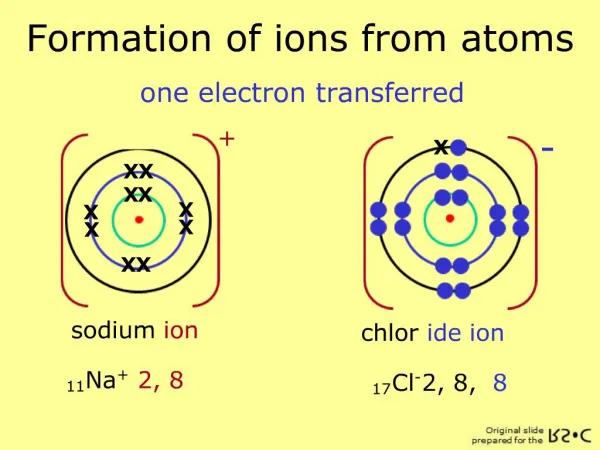
Atome Na neutron (K)2(L)8(M)1 proton 1 e- externe électron La formation des ions L’atome perd 1 e- Na Sodium Z = 11 et il forme l’ion Na+
Atome Na neutron (K)2(L)8(M)1 (K)2(L)8 proton 8 e- externes 1 e- externe électron Structure en octet La formation des ions Ion Na+ Na Sodium Z = 11
Li+, Na+, K+ La formation des ions Les éléments de la famille des alcalins forment des cations qui portent 1 charge positive
La formation des ions Exemple de la famille des alcalino-terreux: le magnésium
Atome Mg neutron (K)2(L)8(M)2 proton 2 e- externes électron La formation des ions Mg Magnésium Z = 12 Comment faire pour appliquer la règle de l’octet ???
Atome Mg neutron (K)2(L)8(M)2 proton 2 e- externes électron La formation des ions L’atome perd 2 e- Mg Magnésium Z = 12 et il forme l’ion Mg2+
Atome Mg neutron (K)2(L)8(M)2 (K)2(L)8 proton 8 e- externes 2 e- externes électron Structure en octet La formation des ions Ion Mg2+ Mg Magnésium Z = 12
Be2+, Mg2+, Ca2+ La formation des ions Les éléments de la famille des alcalino-terreux forment des cations qui portent 2 charges positives
La formation des ions Exemple de la famille des halogènes: le chlore
Atome Cl neutron (K)2(L)8(M)7 proton 7 e- externes électron La formation des ions Cl Chlore Z = 17 Comment faire pour appliquer la règle de l’octet ???
Atome Cl neutron (K)2(L)8(M)7 proton 7 e- externes électron La formation des ions L’atome gagne 1 e- Cl Chlore Z = 17 et il forme l’ion Cl-
Atome Cl neutron (K)2(L)8(M)7 (K)2(L)8(M)8 proton 8 e- externes 7 e- externes électron Structure en octet La formation des ions Ion Cl- Cl Chlore Z = 17
F-, Cl- La formation des ions Les éléments de la famille des halogènes forment des anions qui portent 1 charge négative
Li+ Be2+ B3+ O2- F- Na+ Mg2+ Al3+ S2- Cl- K+ Ca2+ La formation des ions Grâce à la classification périodique et à la règle de l’octet, on sait prédire quels ions vont former les différents éléments chimiques.
FIN G. Baudot (http://www.nanomega.free.fr) – Lycée Victor Hugo – Carpentras - 2007