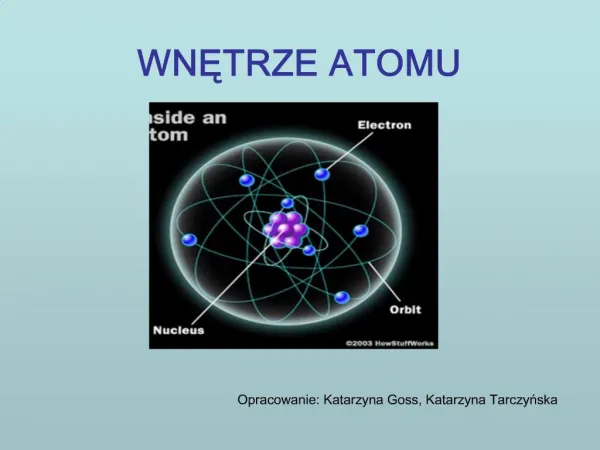
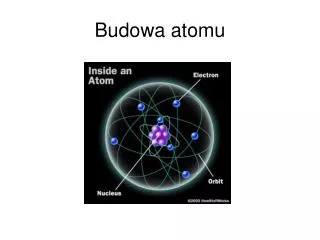
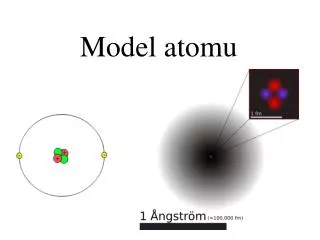
Stavba atomu
Stavba atomu. CH-1 Obecná chemie, DUM č. 3. Mgr. Radovan Sloup. 1. ročník čtyřletého studia. Gymnázium Sušice. Tento materiál byl vytvořen v rámci projektu Gymnázium Sušice – Brána vzdělávání II. STAVBA ATOMU. Démokritos starověk -. hmota se dělí na vodu, vzduch, oheň. obr.1.


Stavba atomu
E N D
Presentation Transcript
Stavba atomu CH-1 Obecná chemie, DUM č. 3 Mgr. Radovan Sloup 1. ročník čtyřletého studia Gymnázium Sušice Tento materiál byl vytvořen v rámci projektu Gymnázium Sušice – Brána vzdělávání II
STAVBA ATOMU Démokritos starověk - hmota se dělí na vodu, vzduch, oheň obr.1 látky jsou z atomů = nedělitelné částice (atomos = nedělitelný) nejmenší částice hmoty, mnoho druhů atomů Demokritos 470 – 360 př.n.l.
STAVBA ATOMU Daltonova atomová teorie (1801) ve třech bodech: atomy jsou nesmírně malé, neměnné a nedělitelné částice, atomy jednoho prvku jsou stejné, atomy různých prvků se liší například hmotností 2. v průběhu chemických reakcí dochází ke spojování, oddělování a přeskupování atomů, atomy při nich nevznikají, nemizí ani se atom jednoho prvku nemění v atom jiného prvku 3. slučováním atomů dvou nebo více prvků vznikají chemické sloučeniny, v určité sloučenině připadá na jeden atom jednoho prvku vždy stejný počet atomů jiného prvku obr.2 John Dalton 1766 - 1844
STAVBA ATOMU John Thomson1904 „pudinkový model atomu“ v atomu jsou dvě části elektrony – záporný náboj polévka - kladný náboj obr.3 e- e- e- e- e- e- e- e- e- e- e- e- e- e- e- e- e- e- e- e- e- e- e- e- e- e- e- pudinkový model atomu John Thomson 1856 - 1940
STAVBA ATOMU obr.5 Ernest Rutherford1911 „planetární model atomu“ jádro – kladný náboj obal – záporný náboj v atomu jsou dvě části obr.4 Ernst Rutherford 1871 - 1937 planetární model atomu
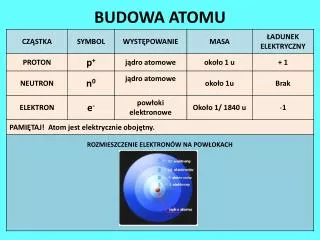
STAVBA ATOMU 1 . 10-10 m, tj. 0,000 000 000 1 m p+ n0 e- = protony = neutrony = elektrony e- p+ n0 protony a neutronyjsou částice jádra neboli nukleony elektronyjsou v obalu
STAVBA ATOMU e- e- e- 6p+ e- e- e- p+ n0 e- = protony = neutrony = elektrony e- p+ n0 v atomu prvku je ! počet protonů a elektronů stejný ! celková hodnota náboje je rovna nule
STAVBA ATOMU p+ n0 e- = protony = neutrony = elektrony nukleonové číslo protonové číslo e– e– e– n0 p+ p+ p+ n0 n0 např. v atomu vodíku jepočet protonů a elektronů stejný ale mění se počet neutronů, vznikají IZOTOPY v atomu prvku je ! počet protonů a elektronů stejný ! celková hodnota náboje je rovna nule
STAVBA ATOMU s pomocí periodické tabulky doplň chybějící údaje:
STAVBA ATOMU řešení:
STAVBA ATOMU Vytvořeno v rámci projektu Gymnázium Sušice - Brána vzdělávání II Autor: Mgr. Radovan Sloup, Gymnázium Sušice Předmět: Chemie (obecná chemie) Třída: první ročník čtyřletého gymnázia Označení: VY_32_INOVACE_Ch-1_03 Vytvořeno: 3.10.2012 Anotace a metodické poznámky Prezentace slouží ke shrnutí tématu „atom a jeho složení“, k procvičení tématu a opakování. V úvodu jsou zmíněny známé modely atomů, jejich vývoj a rozdíly. Tyto informace nejsou většinou v současných učebnicích k dispozici. Elementární stavba atomu je shrnuta v závěru cvičením formou doplnění tabulky. Tuto tabulku žáci vyplňují s pomocí periodické tabulky prvků. Před vyplňováním tabulky musí žáci dostat informaci o tom, že vodík většinou nemá v jádru neutron. Tabulku lze vytisknout k písemnému testování, případně rozšířit. Použité materiály: Honza, J.; Mareček, A.; Chemie pro čtyřletá gymnázia (1.díl).Brno: DaTaPrint, 1995;ISBN 80-900066-6-3 Vacík, J. a kol.; Chemie pro I. ročník gymnázií. Praha: SPN, 1984; ISBN 80-04-25219-4 obr.1 Demokritos (2:10:2012), autor Rubens: http://commons.wikimedia.org/wiki/File:Rubens-democrito-prado.jpg obr.2 Dalton (28.9.2012) autor Schuster & London: http://commons.wikimedia.org/wiki/File:SS-dalton.jpg obr.3 Thomson (28.9.2012) autor neznámý: http://commons.wikimedia.org/wiki/File:PSM_V78_D529_Joseph_John_Thomson.png obr.4 Rutherford (28.9.2012) autor neznámý: http://commons.wikimedia.org/wiki/File:Ernest_Rutherford.jpg obr.5 model atomu (28.9.2012) autor Debianux: http://commons.wikimedia.org/wiki/File:ScientificLinux-Logo.gif ostatní obrázky jsou materiálem autora prezentace Vše je vytvořeno pomocí nástrojů Power Point 2003, Word (WordArt) 2003 Materiály jsou určeny pro bezplatné používání pro potřeby výuky a vzdělávání na všech typech škol a školských zařízení. Jakékoliv další využití podléhá autorskému zákonu.