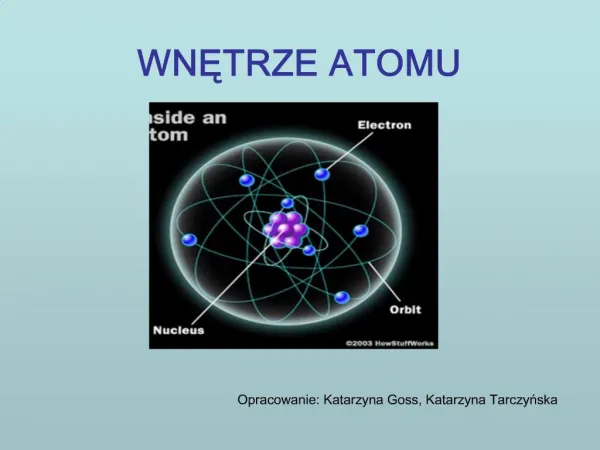
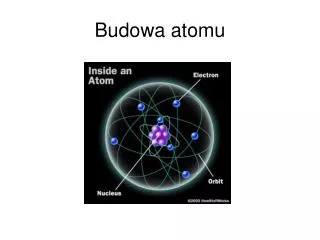
Modely atomu
Modely atomu. Demokritos 460 – 370 př.n.l. Isaac Newton 1643 – 1727. Pierre Gassendi 1592 – 1655. Myšlenka, že látka není spojitá, má strukturu a skládá se z atomů pochází z antiky. Propagovali ji filozofové jako Demokritos, Epikuros a další.

Modely atomu
E N D
Presentation Transcript
Modely atomu Demokritos 460 – 370 př.n.l. Isaac Newton 1643 – 1727 Pierre Gassendi 1592 – 1655 Myšlenka, že látka není spojitá, má strukturu a skládá se z atomů pochází z antiky. Propagovali ji filozofové jako Demokritos, Epikuros a další. Na antický atomismus navazovali mnozí filozofové a fyzikové novověku, např. francouzský matematik a astronom Pierre Gassendi nebo Isaac Newton. Pro své domněnky však neměli jediný důkaz.
Modely atomu O C O C O John Dalton 1766 – 1844 Joseph L. Proust 1754 – 1826 CO CO2 V devatenáctém století nastupuje atomismus chemický. Francouzský chemik J. Proust při studiu redukčně-oxidačních reakcí zjistil, že látky se slučují jen v určitých hmotnostních poměrech. Anglický chemik J. Dalton dále zjistil, že některé chemické prvky se mohou slučovat i ve více poměrech. Obě tyto zákonitosti (Zákon stálých poměrů slučovacích, Zákon násobných poměrů slučovacích) lze vysvětlit tak, že prvky se skládají z atomů a sloučeniny z molekul – spojení několika atomů.
Modely atomu Joseph L. Gay-Lussac 1778 – 1850 Amadeo Avogadro 1776 – 1856 Hypotézu atomů potvrdily i další objevy. Francouzský fyzik J. L. Gay-Lussac přišel na další zákon chemického slučování. Zjistil, že slučují-li se některé plyny, vstupují do reakce vždy jejich stejné nebo násobné objemy. To se dá vysvětlit tak, že ve stejných objemech různých plynů je stejný počet atomů. Ve zbylých případech se objem plynů mění – např. při slučování jednoho dílu chloru a jednoho dílu vodíku vznikají dva díly chlorovodíku. Tuto nejasnost vysvětlil italský fyzik a chemik Avogadro zákonem který říká, že ve stejných objemech různých plynů je při stejném tlaku a teplotě vždy stejný počet molekul. Přitom předpokládal, že některé prvky v plynném stavu nejsou jednoatomové, ale jsou tvořeny molekulami (např. H2 či Cl2, které pak dají vzniknout dvěma molekulám HCl).
Objev elektronu Katodové paprsky
Objev elektronu Joseph J. Thompson 1856 - 1940 J. J. Thompson je pokládán za objevitele první elementární částice, elektronu. Spolu s Millikanem určili základní vlastnosti této částice – náboj a hmotnost. Robert Millikan 1868 - 1953 J. J. Thompson roku 1897 vysvětlil katodové paprsky pomocí proudu nabitých částic, jakýchsi „částeček elektřiny“. Pro tyto částice se ujal název elektron. Ze zakřivení drah elektronů v magnetickém poli určil Thompson měrný náboj elektronu, tj. veličinu e/me . Americký fyzik R. Millikan prováděl v roce 1910 řadu pokusů k určení hodnoty elektrického náboje elektronu, tzv. elementárního náboje. Spolu s hodnotou e/m pak bylo možné usoudit na hmotnost elektronu.
Měření e/m B R e- U
Millikanův experiment Olejové kapičky Nabité desky Fe Fg
Objev atomového jádra Ernest Rutherford 1871 - 1937 e- e- e- e- e- e- e- e- Poznatek, že elektrony vyletují z atomů vyvrátil odvěkou představu o nedělitelnosti a nastolil otázku jejich struktury. J. J. Thompson se domníval, že kladný náboj je rovnoměrně rozložen v celém objemu atomu a elektrony v něm vězí jako rozinky v pudingu. Tuto hypotézu vyvrátili roku 1911 E. Rutherford a jeho spolupracovníci ve slavném experimentu rozptylu záření α na tenké zlaté fólii.
Objev atomového jádra Rozptýlené α částice Proud α částic Scintilátor Tenká zlatá fólie Lehce rozbíhavý kužel Předpověď výsledku Rutherfordova pokusu, kdyby platila Thompsonova rozinková teorie stavby atomu.
Rutherfordův pokus Atom se skládá z malého, kladně nabitého jádra, ve kterém je soustředěna téměř veškerá hmotnost atomu, zabírá však minimální zlomek jeho celkového objemu. Kladný náboj jádra a záporný náboj elektronového obalu se navzájem ruší.
Planetární model atomu V návaznosti na Rutherfordův pokus byl atom popisován pomocí planetárního modelu. Jádro zde fungovalo jako slunce, kolem nějž po kruhových orbitách létaly elektrony. Jejich přitažlivost ovšem nebyla dána gravitační interakcí, nýbrž elektromagnetickou. Dle klasické elektrodynamiky nabitá částice, která se pohybuje se zrychlením, vyzařuje elektromagnetické vlny a ztrácí tak energii. Klasická fyzika tedy předpovídala, že elektrony musí velmi rychle ztratit pohybovou energii a spadnout na jádro. Tento paradox nebylo možno vysvětlit bez pomocí kvantové teorie.
Bohrův model atomu Niels Bohr 1885 - 1962 Destruktivní interference na kruhovém orbitu Stojatá vlna na kruhovém orbitu Dánský fyzik Niels Bohr v roce 1913 použil závěrů kvantové mechaniky, že částici lze popsat jako vlnu. V jeho modelu atomu se elektrony mohou držet vždy na přesně daných kruhových orbitech, a to na takových, kde mohou vytvořit stojaté vlnu. Tam, kde by výsledná interference byla destruktivní se elektrony nalézat nemohou. Proto není možné, aby po spirále spadly na jádro a atom zůstává stabilní.
Bohrův model atomu Na základě Bohrova modelu bylo možné vysvětlit, proč se spektra, která emitují vybuzené atomy, skládají z diskrétních čar. Na každém orbitu má elektron specifickou energii. Při přechodu mezi orbity ji musí pohltit nebo vyzářit ve formě fotonu. A jelikož jsou orbity diskrétní, rozdíly energií mezi nimi jsou přesně dané. Elektrony při přechody mezi orbity (hladinami) vyzařují nebo přijímají vždy stejné a přesně dané množství energie. V příslušných spektrech jsou pak jen určité diskrétní barvy.