Na+
Na+. Na+. P-. הפוטנציאל האלקטרוכימי. אנרגיה חופשית ל- 1 mole חומר. מרכיבי הפוטנציאל האלקטרוכימי של חומר X :. מרכיב כימי. מרכיב חשמלי. m ניתן ביחידות של joul/mole. המרכיב הכימי : RTlnC x R – קבוע הגזים ( R=8.314 joul/mole* o K ) T – טמפרטורה מוחלטת ( o K=t o C+273 )

Na+
E N D
Presentation Transcript
Na+ Na+ P-
הפוטנציאל האלקטרוכימי אנרגיה חופשית ל- 1 mole חומר. מרכיבי הפוטנציאל האלקטרוכימי של חומר X: מרכיב כימי מרכיב חשמלי m ניתן ביחידות של joul/mole המרכיב הכימי: RTlnCx R – קבוע הגזים (R=8.314 joul/mole*oK) T – טמפרטורה מוחלטת (oK=toC+273) Cx- הריכוז של x (ביחידות של M=mole/liter) המרכיב החשמלי: ZxFy Zx – הערכיות של x F – מספר פרדיי Faraday(coulomb / mole) y– הפוטנציאל החשמלי (יחידות – volt)
כעת נבדוק מהו הפרש הפוטנציאלים של x משני צידי הממברנה: זו הצורה המקובלת להצגת הפוטנציאל האלקטרוכימי של חומר x משני צידי הממברנה. עבור חומר x, הנמצא משני צידי ממברנה, נגדיר את הפוטנציאל האלקטרוכימי משני הצדדים:
זהו פוטנציאל שווי המשקל של יון (x) שנקרא גם פוטנציאל נרנסט של יון – Nernst potential. עבור יון חד ערכי (Zx=+1) ניתן לכתוב גם: 58mV כאשר החומר X נמצא בשווי-משקל משני צידי הממברנה: ואז:
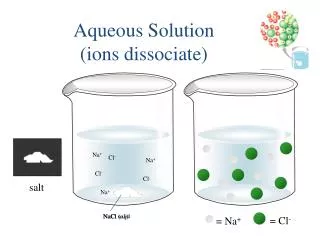
מתקיים: כלומר, פוטנציאל נרנסט (פוטנציאל שווי המשקל) של כל יון, שווה לפוטנציאל החשמלי הנמדד של המערכת. לדוגמא, במערכת בשווי משקל, המכילה יוני Na+ ויוני Cl-: ניתן לכתיבה גם כפי שנוסח ע"י דונאן ("מכפלת דונאן"): כאשר המערכת כולה נמצאת בשווי משקל: עבור כל חומר x:
עקרון האלקטרוניטרליות – ריכוז המטענים החיובים והשליליים בכל מדור שווה! (ברמה המקרוסקופית)
א' א' ב' ב' 100mM NaCl 100mM NaCl 10mM NaCl 1mM NaCl כוח ריכוזי אם נציב במשוואת נרנסט: Dji-o = 58*log(100/10) = 58mV כוח חשמלי ג. הממברנה חדירה ליוני נתרן בלבד ומפל ריכוזי היון גדול יותר: Dji-o = 58*log(100/1) = 116mV כוח ריכוזי אפשר לראות שבמעבר מ-ב' ל-ג' מפל הריכוזים גדל פי 10 והפוטנציאל החשמלי גדל פי 2. כוח חשמלי דוגמאות א. מה יקרה אם הממברנה חדירה לשני היונים במידה שווה? אם נציב במשוואת נרנסט: Dji-o = 58*log(55/55) = 0 ב. מה יקרה אם הממברנה חדירה ליוני נתרן בלבד?
ניתן להיעזר במשוואת דונן או במשוואת נרנסט: Dji-o = 0 = 58*log(Ho/Hi) או Hout/Hin = Clin/Clout וגם באופן אינטואיטיבי ברור שה-pH הפנימי, במקרה זה, זהה לחיצוני. Ho*Clo לפי דונן: Hi= =1.68*10-7M Cli כלומר:pHin = 6.77 כדוריות דם אדומות נמצאות בתוך תמיסת HCl. נתון: pHout = 7Clin/Clout= 1Dji-o = 0 מה ה-pH בתוך הכדוריות, בהנחה שהמערכת הגיעה לשווי משקל? העבירו את הכדוריות לתמיסה שונה, וגם בה המערכת הגיעה לשווי משקל. נתון: pHout = 6.6Clin/Clout= 1.49Dji-o = +10mV מה ה-pH הפנימי הפעם?
Clo=Ho=2.51*10-7M Cli=3.74*10-7M Hi=1.68*10-7M הצגנו מערכת בשווי-משקל בה: האם עקרון האלקטרוניטרליות נשמר במערכת זו? אם כן, הכיצד? מדוע מתקבל פוטנציאל חיובי בתוך הכדוריות?
שווי משקל – איזון בין כוחות הפוכים מצב עמיד – המצב לא משתנה לאורך זמן Vm = -66mV ENa+ = 58*log([Na+]out/[Na+]in) = 58*log(150/15) = 58mV EK+ = 58*log([K+]out/[K+]in) = 58*log(5.5/150) = -83mV ECl- = -58*log([Cl-]out/[Cl-]in) = -58*log(125/9) = -66mV