METABOLISMO DEL FERRO
650 likes | 1.41k Vues
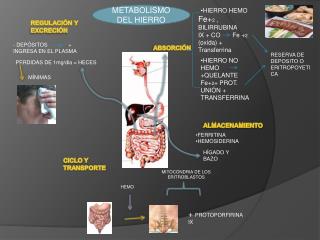
METABOLISMO DEL FERRO. Cammini biologici in cui è coinvolto il ferro. Respirazione (Trasposto O 2 e catena respiratoria) Sintesi del DNA (Ribonucleotide riduttasi) Proliferazione cellulare ( cyclin dependent kinases ) Risposta all’ipossia (HIF)

METABOLISMO DEL FERRO
E N D
Presentation Transcript
Cammini biologici in cui è coinvolto il ferro • Respirazione (Trasposto O2 e catena respiratoria) • Sintesi del DNA (Ribonucleotide riduttasi) • Proliferazione cellulare (cyclin dependent kinases) • Risposta all’ipossia (HIF) • Infiammazione (ciclo ossigenasi, Adenilato ciclasi) • Sintesi di ormoni(Triptofano ossigenasi) • Sintesi NO (NO sintasi) • Attività anti-ossidante (Catalasi, SOD, perossidasi) • altro
Distribuzione di Fe nell’organismo 3-5 g/70 kg: • 68% in Emoglobina • 4% in Mioglobina • 0.1% in Transferrina • 27% in Ferritina tissutale • 0.004% in Ferritina plasmatica • 0.6% in vari enzimi
Distribuzione del ferro nell’uomo Ferro totale: 4-6 g Scambi : 1-2 mg/die Ferro-transferrina: 3 mg • Assorbimento del ferro • Avviene nel duodeno, circa 10% del totale, è influenzato da • Quantità e biodisponibilita’ del ferro nella dieta • Dai depositi organici di ferro • Velocità di eritropoiesi • Ipossia dei tessuti
Movimenti del ferro • La transferrina cede il ferro a tutti i tessuti, ed in particolare ai precursori eritroidi • I depositi organici del ferro sono principalmente nel fegato, epatociti, nelle molecole di ferritina. • L’assorbimento del ferro è regolato dal fegato (storage regulator) e dal midollo osseo (erithroid regulator)
Forme biologicamente rilevanti • Fe+++ (ione ferrico) • Prevalente a pH alcalino e neutro • Forma complessi insolubili con OH- e anioni • Fe++ (ione ferroso) • Prevalente a pH acido • Buona solubilità • Facilmente ossidabile a Fe+++ • Il passaggio di Fe da una molecola M1 ad un’altra M2 deve essere preceduto dal cambiamento di valenza, catalizzato da ferroxidasi M1- Fe+++ M1 - Fe++ M1 + Fe++ M2 + Fe++ M2 - Fe++ M2 - Fe+++
Assorbimento Poco efficiente Normale: <10% In caso di deficit di Fe: 30% Fabbisogno: 1 mg/die per soggetti sani e normali 3 mg/die per donne mestruanti 3-6 mg/die durante gravidanza e allattamento Escrezione Per via urinaria e sudorifera: poco efficiente Via primaria di escrezione: perdita di cellule Epidermide Mucosa intestinale, 1 mg/die Sangue: mestruo (0.5-1 g/die) emorragie, versamenti etc Assorbimento duodenale e escrezione di Fe
Il ferro nella dieta • Alimenti ricchi in Fe: • Carni, legumi, frutta, cereali • Cottura = rottura legami Fe-proteina • Facilita l’assorbimento • pH acido nello stomaco: Fe+++ Fe++ • Ulcera gastrica impedisce l’assorbimento di Fe anemia • Ascorbato: Fe+++ Fe++ • Braccio di Ferro ha sbagliato tutto: gli spinaci contengono Fe, ma come Fe-fitato, resistente all’azione chimica!
Understanding Heme Transport - N.C Andrews - New England Journal of Medicine:353;23 - 2508
Il ciclo della transferrina La Fe-transferrina si lega al recettore (TfR) Il complesso è internalizzato negli endosomi, a pH acido Il ferro è rilasciato e trasportato nel citosol da DMT1 Esso è usato per la sintesi di enzimi e depositato nella ferritina
Ferritina • 24 subunità: • H (Heavy o Heart) • L (Light o Liver) • 25 isoforme: • L24 in fegato e milza • H24 in tessuti fetali, neoplastici, cuore, placenta • Sfera con cavità centrale • Contiene fino a 4500 Fe+++ (sali di fosfato e idrossidi) • Saturazione di Ft per Fe: • Normalmente 50-70%, ma dipende dallo stato di sovraccarico o deficit di Fe+++ • Fe+++ in eccesso si deposita in aggregati insolubili chiamati emosiderina • Abbondante nella mucosa intestinale • Ft nel siero: • Marker dei depositi di Fe nell’organismo • Proteina di fase acuta • Marker di malnutrizione
Ferritina Mitocondriale La ferritina mitocondriale (MtF), è codificata da un gene senza introni sul cromosoma Il precursore è una proteina di 242 amino acidi che è processata nel mitocondria nella forma matura che assemble in ferritina funzionale con attività ferroxidasica Ha proprietà di iron storage Ha una espressione strettamente tessuto specifica (testis, islets of Langherans, neurons?)
Traffico del Ferro nel mitocondrio Il Fe è incorporato nell’eme dalla Ferrochelatasi mitocondriale Il Fe è incorporato nei centri Fe/S da una complessa serie di passaggi mitocondriali Può essere depositato nella ferritina mitocondriale L’ingresso forse coinvolge i trasportatori mitoferrins L’uscita il trasportatore ABC7 (per Fe/S) ed altri
Transferrina (Tf) • -glicoproteina, sintetizzata in fegato, 78 kDa • 2 siti di legame con Fe+++, 3 forme: • Tf o apoTf: 44% • Tf - Fe: 44% • Tf-2 Fe: 11% • Cofattore: HCO3- • Altissima affinità, Keq=1019-1031 M-1: • In presenza di Tf, non esiste Fe+++ libero • Tf-2Fe+++ internalizzata nelle cellule eritroidi e placenta
Cellule specializzate nel rilascio del ferro: enterociti e macrofagi Gli enterociti rilasciano 1-2 mg Fe/die, i macrofagi 20-30 mg/die
Meccanismo di trasporto cellulare di ferro mediato dalla transferrina Il meccanismo di trasporto del Fe all’interno degli entrociti è un esempio diendocitosi mediata da un recettore. La metalloproteina si unisce a un recettore specifico della membrana (che non ha affinità per l’apotranferrina). La parte interna della stessa si ricopre con un reticolo formato da una proteina chiamata clatrina, che aiuta a formare prima una borsa e poi una vescicola (endosoma), la cui membrana contiene pompe protoniche che consumano ATP e sono capaci di modificare il pH interno fino a portarlo a un valore fra 5,5 e 6. In queste condizioni la metalloproteina, perde il ferro, che si sposta fino al citosol probabilmente attraverso un trasportatore specifico. Una volta lì esso può essere immagazzinato come ferritina o essere utilizzato nei mitocondri per sintetizzare gruppi eme. La apotransferrina, ancora nella vescicola, si diffonde nuovamente verso il plasma dove viene liberata a opera del recettore e può tornare a cominciare il ciclo.
Regolazione molecolare del deficit/sovraccarico di Fe • Iron Regulatory Protein (IRP o aconitasi) risponde a [Fe] • Si lega a Iron Responsive Element (IRE) su mRNA di • Ferritina • Recettore di Tf
Sul gene di ferritina IRP destabilizza mRNA di Ft Diminuzione di Ft Aumento di assorbimento intestinale di Fe Sul gene del recettore di Tf IRP stabilizza mRNA Aumento di espressione del recettore di Tf Aumento dell’internalizzazione di Fe Effetto del deficit di Fe
Sul gene di ferritina IRP stabilizza mRNA di Ft Aumento di Ft Diminuzione dell’assorbimento intestinale di Fe Sul gene del recettore di Tf IRP destabilizza mRNA Diminuzione di espressione del recettore di Tf Diminuzione dell’internalizzazione di Fe Effetto del sovraccarico di Fe
Fase asintomatica: Riduzione dei depositi di Fe epatici e nel midollo osseo Gli indici sideremia e saturazione della Tf permangono normali Fase sintomatica: Riduzione di Hb circolante, anemia (diventa evidente solo dopo che le riserve di Fe si sono esaurite!) Cambiamenti morfologici dell’eritrocita (microcitemia, ipocromocitemia) Diminuzione della saturazione Tf Aumento di Tf (risposta tendente ad aumentare l’assorbimento dall’intestino) Di origine genetica (emocromatosi idiopatica): Incidenza del gene: 10% della popolazione USA di origine celtica Incidenza della patologia (0.25% della popolazione) Colpisce prevalentemente gli individui maschi Di origine alimentare Consumo eccessivo di carne e alcool Di origine patologica Anemie, -talassemia e anemie emolitiche Soggetti politrasfusi Alcolizzati cronici Fisiopatologia del deficit e sovraccarico di ferro