พันธะ โคเวเลนต์ Covalent Bond
พันธะ โคเวเลนต์ Covalent Bond. การเปลี่ยนแปลงพลังงานในการเกิดโมเลกุลไฮโดรเจน. พลังงานศักย์ ( kJ/mol). H. H. H. H. 436 kJ/mol. ระยะระหว่างอะตอมของไฮโดรเจน ( pm). 74 pm. นิยาม.

พันธะ โคเวเลนต์ Covalent Bond
E N D
Presentation Transcript
พันธะโคเวเลนต์ Covalent Bond
การเปลี่ยนแปลงพลังงานในการเกิดโมเลกุลไฮโดรเจนการเปลี่ยนแปลงพลังงานในการเกิดโมเลกุลไฮโดรเจน พลังงานศักย์ (kJ/mol) H H H H 436 kJ/mol ระยะระหว่างอะตอมของไฮโดรเจน (pm) 74 pm
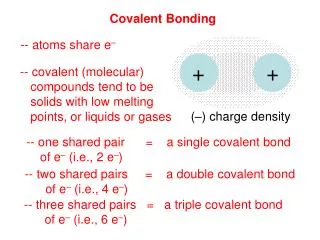
นิยาม พันธะโคเวเลนต์ ( Covalent bond ) หมายถึง พันธะที่เกิดจากอะตอมคู่หนึ่งใช้อิเล็กตรอนร่วมกัน โดยเกิดแรงดึงดูดระหว่างอิเล็กตรอนกับโปรตอนในนิวเคลียสของอะตอมทั้งสอง IE สูง กับ IE สูง หรือ อโลหะ กับ อโลหะ
ชนิดของพันธะโคเวเลนต์ชนิดของพันธะโคเวเลนต์ I I I I I 1 อะตอม I2โมเลกุล I 1 อะตอม O O O O O 1 อะตอม O2โมเลกุล O 1 อะตอม N N N N N 1 อะตอม N2โมเลกุล N 1 อะตอม
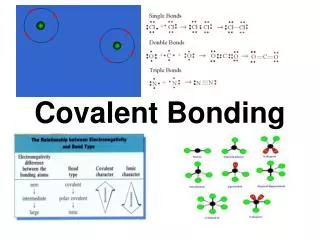
I I I2โมเลกุล O O O2โมเลกุล N N N2โมเลกุล I I พันธะเดี่ยว eคู่ร่วมพันธะ 1 คู่ (Single bond) O O พันธะคู่ eคู่ร่วมพันธะ 2 คู่ (Double bond) N N พันธะสาม (Triple bond) eคู่ร่วมพันธะ 3 คู่
O O O O พันธะโคออร์ดิเนตโคเวเลนต์ (Coordinate Covalent bond หรือ Dative Covalent bond) พันธะโคออร์ดิเนตโคเวเลนต์ พันธะโคเวเลนต์ O O O O O O3
นิยาม พันธะที่เกิดขึ้นโดยอิเล็กตรอนคู่ร่วมพันธะมาจากอะตอมของธาตุเดียว ส่วนอีกธาตุหนึ่งไม่ได้ส่งอิเล็กตรอนมาร่วมพันธะแต่มาใช้อิเล็กตรอนคู่โดดเดี่ยวของธาตุอื่น เพื่อให้จำนวนเวเลนต์อิเล็กตรอนครบ 8 ตามกฎออกเตต
การเขียนสูตรแบบเส้นและแบบจุดการเขียนสูตรแบบเส้นและแบบจุด 1. หาอะตอมกลาง 2. วางตำแหน่งของอะตอมของธาตุทั้งหมด 3. เขียนสูตรแบบเส้นและแบบจุด ตามลำดับ
โครงสร้างแบบจุดอิเล็กตรอนโครงสร้างแบบจุดอิเล็กตรอน • การเขียนโครงสร้างลิวอิสหรือโครงสร้างแบบจุดอิเล็กตรอน (Lewis’sdot structure) เป็นวิธีการเขียนเพื่อแสดงวาเลนซ์อิเล็กตรอนและการสร้างพันธะโควาเลนต์ระหว่างอะตอมในโมเลกุล • โครงสร้างลิวอิสของอะตอม • ใช้จุดแทนวาเลนซ์อิเล็กตรอน
H H C H H H HCH H NN N N โครงสร้างลิวอิสของโมเลกุล • โครงสร้างลิวอิสของโมเลกุล • พันธะโควาเลนต์คือการใช้อิเล็กตรอนร่วมกันของสองอะตอม • หนึ่งพันธะประกอบด้วยสองอิเล็กตรอน (2 shared electrons) • แต่ละพันธะแทนด้วยจุด 2 จุด (:) หรือ หนึ่งเส้น () • อิเล็กตรอนที่ใช้ในการสร้างพันธะ เรียกว่า bonding electron • อิเล็กตรอนที่ไม่เกี่ยวข้องกับการสร้างพันธะเรียกว่า non-bonding electron
การเขียนโครงสร้างลิวอิสการเขียนโครงสร้างลิวอิส • กำหนดอะตอมกลาง(ต้องการ valence electron หลายตัว) และการจัดเรียงอะตอมในโมเลกุล • นับจำนวนเวเลนซ์อิเล็กตรอนของทุกอะตอมในโมเลกุล • ไอออนลบ: เพิ่มจำนวนอิเล็กตรอนเท่ากับจำนวนประจุลบของไอออน • ไอออนบวก: ลบจำนวนอิเล็กตรอนเท่ากับจำนวนประจุบวกของไอออน • เชื่อมอะตอมด้วยพันธะเดี่ยว(ระหว่างอะตอมกลางกับอะตอมปลาย) โดยใช้ 2 อิเล็กตรอนในการสร้างพันธะเดี่ยวแต่ละพันธะ • เติมวาเลนซ์อิเล็กตรอนให้กับอะตอมปลายให้ครบ8 (ยกเว้น H เท่ากับ 2) • เติมอิเล็กตรอนที่เหลือให้กับอะตอมกลาง (อาจมากกว่า 8) • ถ้าจำนวนวาเลนซ์อิเล็กตรอนที่อะตอมกลางไม่ครบ 8 ให้นำอิเล็กตรอนที่ไม่ร่วมพันธะของอะตอมรอบๆ มาสร้างพันธะคู่หรือพันธะสาม • จำนวนวาเลนซ์อิเล็กตรอนรวมต้องเท่ากับที่ได้จากข้อ 1.
หรือ F N F F F N F F F N F F F N F F F N F F F N F F หรือ หรือ ตัวอย่างโครงสร้างลิวอิสของ NF3 1. อะตอมกลางคือ N 2. จำนวนเวเลนซ์อิเล็กตรอน = 5 + (7x3) = 26 อิเล็กตรอน(จำนวนเวเลนซ์อิเล็กตรอนของ N= 5 F = 7) 3. เขียนพันธะเดี่ยวระหว่างอะตอมกลางกับอะตอมปลาย 4. เขียนอิเล็กตรอนของอะตอมปลายให้ครบ 8 5. เติมอิเล็กตรอนที่เหลือให้กับอะตอมกลาง (26-24 = 2 อิเล็กตรอน)
H C N H C N H C N H C N HCN ตัวอย่าง โครงสร้างลิวอิสของ HCN • อะตอมกลางคือ C • จำนวนเวเลนซ์อิเล็กตรอนของ HCN 1 + 4 + 5 =10 อิเล็กตรอน • เขียนพันธะเดี่ยวระหว่างอะตอมกลางกับอะตอมที่มีพันธะ • เขียนอิเล็กตรอนของอะตอมปลาย ให้ครบ 8 (หรือ 2) • เติมอิเล็กตรอนที่เหลือให้กับอะตอมกลาง (10-10 = 0)ยังไม่เป็นไปตามกฎออกเตต • นำอิเล็กตรอนที่ไม่ร่วมพันธะของอะตอมรอบๆ (N) มาสร้างพันธะคู่หรือพันธะสาม จนอะตอมกลางมีอิเล็กตรอนครบแปด
หรือ F N F F F N F F F N F F F N F F F N F F F N F F หรือ หรือ ตัวอย่างโครงสร้างลิวอิสของ NF3 1. อะตอมกลางคือ N 2. จำนวนเวเลนซ์อิเล็กตรอน = 5 + (7x3) = 26 อิเล็กตรอน(จำนวนเวเลนซ์อิเล็กตรอนของ N= 5 F = 7) 3. เขียนพันธะเดี่ยวระหว่างอะตอมกลางกับอะตอมปลาย 4. เขียนอิเล็กตรอนของอะตอมปลายให้ครบ 8 5. เติมอิเล็กตรอนที่เหลือให้กับอะตอมกลาง (26-24 = 2 อิเล็กตรอน)
H C N H C N H C N H C N HCN ตัวอย่าง โครงสร้างลิวอิสของ HCN • อะตอมกลางคือ C • จำนวนเวเลนซ์อิเล็กตรอนของ HCN 1 + 4 + 5 =10 อิเล็กตรอน • เขียนพันธะเดี่ยวระหว่างอะตอมกลางกับอะตอมที่มีพันธะ • เขียนอิเล็กตรอนของอะตอมปลาย ให้ครบ 8 (หรือ 2) • เติมอิเล็กตรอนที่เหลือให้กับอะตอมกลาง (10-10 = 0)ยังไม่เป็นไปตามกฎออกเตต • นำอิเล็กตรอนที่ไม่ร่วมพันธะของอะตอมรอบๆ (N) มาสร้างพันธะคู่หรือพันธะสาม จนอะตอมกลางมีอิเล็กตรอนครบแปด
Cl Be Cl โมเลกุลที่ไม่เป็นไปตามกฎออกเตต 1. อะตอมของธาตุในโมเลกุลที่มีเวเลนต์อิเล็กตรอนน้อยกว่า 8 ได้แก่ สารประกอบธาตุคู่ของ Be B และ Al เช่น BeCl2 AlF3 F Al F F
F F F P F F Cl Cl Cl S Cl Cl Cl 2. อะตอมของธาตุในโมเลกุลที่มีเวเลนต์อิเล็กตรอนมากกว่า 8 ได้แก่ สารประกอบธาตุคู่ที่มีอะตอมกลางของธาตุตั้งแต่หมู่ 4 ขึ้นไป เช่น PF5 SCl6
O N O O Cl O 3. ออกไซด์ของธาตุบางชนิด เช่น NO2 ClO2
F F S F F ข้อยกเว้นของกฎออกเตด 1. โมเลกุลที่มีอิเล็กตรอนเป็นเลขคี่ เช่น • ClO2 มีอิเล็กตรอนรวม เท่ากับ 19 • NO มีอิเล็กตรอนรวม เท่ากับ 11 • NO2มีอิเล็กตรอนรวม เท่ากับ 17 2. โมเลกุลที่อะตอมกลางมีอิเล็กตรอนน้อยกว่า 8 • BF3B มีอิเล็กตรอนเท่ากับ 6 • BeH2 Be มีอิเล็กตรอนเท่ากับ 6 3.โมเลกุลที่อะตอมกลางมีอิเล็กตรอนมากกว่า 8 • PCl5มีอิเล็กตรอน เท่ากับ 10 • XeF4มีอิเล็กตรอน เท่ากับ 12 • SF4 มีอิเล็กตรอน เท่ากับ 10
ประจุฟอร์มาล: มักใช้กับการพิจารณาสารโคเวเลนต์ซึ่งถือว่าพันธะที่ยึดอะตอมเข้าด้วยกันเป็นผลจากการใช้เวเลนซ์อิเล็กตรอนร่วมกัน แม้ว่าบางกรณีสารโคเวเลนต์นั้นจะมีประจุรวมเป็นศูนย์ แต่เมื่อพิจารณาเป็นอะตอม อะตอมแต่ละตัวอาจมีประจุเป็นศูนย์ ในขณะที่บางอะตอมเสมือนว่ามีอิเล็กตรอนเกินมา ก็จะมีประจุเป็นลบ และขณะที่บางอะตอมอาจเสมือนว่าเสียอิเล็กตรอนไป ก็จะมีประจุเป็นบวก ซึ่งเรียกประจุเหล่านี้ว่า ประจุฟอร์มาล (formalcharge)
ประจุฟอร์มาล (Formal charge) ประจุฟอร์มาลเป็นความแตกต่างระหว่างจำนวนเวเลนซ์อิเล็กตรอนของอะตอมเดี่ยวกับของอะตอมในโครงสร้างลิวอิสเป็นการทำนายการสภาพขั้วของโมเลกุลอย่างคร่าว ๆ การคำนวณประจุฟอร์มาลของอะตอม • V จำนวนเวเลนซ์อิเล็กตรอนของอะตอมเดี่ยว(อะตอมที่สนใจ) • N จำนวนเวเลนซ์อิเล็กตรอนที่ไม่ได้สร้างพันธะ • B จำนวนอิเล็กตรอนทั้งหมดที่สร้างพันธะรอบอะตอมนั้น
H H O HNCC H H O OIO O +2 1 1 OIO O 1 + - ตัวอย่าง จงหาประจุฟอร์มาลของแต่ละอะตอม • [IO3]– • I = 7 – 2 – ½ (6) = +2 • O = 6 – 6 – ½ (2) = -1 ประจุรวม = +2 – 1 – 1 – 1= -1 • [NH3CH2COO]– วิธีลัด ดูจำนวนพันธะเปรียบเทียบกับจำนวนพันธะที่ควรจะมีของแต่ละอะตอม เช่น N มีวาเลนซ์ 5 ควรมีพันธะ 3 พันธะ ถ้ามีเกินจะเป็นบวก ถ้ามีไม่ครบจะเป็นลบ
.. .. .. .. .. .. .. .. O O O O O O .. .. .. .. - คำนวณประจุฟอร์มาลของ O3 0 +1 -1 O = 6 – 4 – ½(4) = 0 O = 6 – 2 – ½(6) = +1 O = 6 – 6 – ½(2) = -1
.. .. .. .. O O S S O O .. .. เรโซแนนซ์ (Resonance) : หมายถึง การใช้โครงสร้างลิวอิสตั้งแต่ 2 โครงสร้างขึ้นไปแทน โมเลกุลใดโมเลกุลหนึ่ง ข้อควรระวัง คือ การจะเป็นโครงสร้างเรโซแนนซ์ได้สารต้องมีการจัดเรียงตัวของอะตอมเหมือนกัน ต่างเพียงการกระจายอิเล็กตรอนในพันธะเท่านั้น เช่น SO2
+1 +1 S O O S O O -1 -1 เรโซแนนซ์(Resonance) ในบางโมเลกุลหรือไอออน สามารถเขียนแบบจำลองของลิวอิสได้มากกว่า 1 แบบ เช่น CO2 และ SO2 เรียกปรากฏการณ์นี้ว่าปรากฏการณ์เรโซแนนซ์โดยต้องมีการจัดเรียงลำดับของอะตอมเหมือนกันเสมอ ต่างกันแต่เพียงการกระจายอิเล็กตรอนในพันธะ +1 -1 +1 -1 OCO O=C=OOCO
+1 +1 O O O O O O -1 -1 O O O 1.278 Å 1.278 Å เรโซแนนซ์ (Resonance) โครงสร้างลิวอิสของ O3จากการทดลองพบว่า ความยาวพันธะระหว่าง O ทั้งสองเท่ากันแสดงว่าโมเลกุล O3 ไม่เกิดพันธะทั้ง 2 แบบ แต่เกิดโครงสร้างที่เรียกว่า โครงสร้างเรโซแนนซ์(Resonance structure)
N N N N N N N N N โครงสร้าง Lewis ที่เป็นไปได้ หลักในการตัดสินว่าโครงสร้างเรโซแนนซ์แบบใด ควรเป็นไปได้มากที่สุดมี หลักการพิจารณาว่าโครงสร้างใดเป็นโครงสร้างที่เป็นไปได้ มากที่สุด มีดังนี้ 1. เป็นไปตามกฎออกเตดมากที่สุด 2. โครงสร้างที่มีประจุฟอร์มาลต่ำที่สุด 3. อะตอมที่มีค่า EN สูงควรมีประจุฟอร์มาลเป็นลบ 4. อะตอมชนิดเดียวกันไม่ควรมีประจุฟอร์มาลตรงข้ามกัน OCO O=C=OOCO CO2 +1 0 -1 0 0 0 -1 0 +1 N3 -2 +1 0 -1 +1 -1 0 +1 -2
การเขียนสูตรโมเลกุลของสารประกอบโคเวเลนต์การเขียนสูตรโมเลกุลของสารประกอบโคเวเลนต์ 1. เขียนสัญลักษณ์ของธาตุเรียงตามลำดับดังนี้ B Si C Sb As P N H Te Se S At I Br Cl O F 2. ระบุจำนวนอะตอมของธาตุในสารประกอบ โดยเขียนตัวเลขไว้มุมล่างขวา 3. ใช้จำนวนอิเล็กตรอนที่แต่ละอะตอมต้องการคูณไขว้กัน และทำให้เป็นอัตราส่วนอย่างต่ำ เช่น CS C2S4CS2 4 2
ตัวอย่างสูตรสารประกอบโคเวเลนต์ตัวอย่างสูตรสารประกอบโคเวเลนต์ NCl3 CO2 NH3 C2H4 HF CH4 H2S PH3 Cl2O ClO3+PO43- H2O
การเรียกชื่อสารประกอบโคเวเลนต์การเรียกชื่อสารประกอบโคเวเลนต์ 1. สารประกอบธาตุคู่ ให้อ่านธาตุตัวหน้าก่อนและตามด้วยธาตุตัวหลังโดยเปลี่ยนท้ายพยางค์เป็นไอด์ (-ide) 2. ระบุจำนวนอะตอมของแต่ละธาตุด้วยจำนวนในภาษากรีก ดังนี้ mono- (1), di-(2), tri-(3), tetra-(4), penta-(5), hexa-(6), hepta-(7), octa-(8), nona-(9), deca-(10) 3. ถ้าธาตุตัวหน้ามีอะตอมเดียวไม่ต้องระบุจำนวนอะตอม แต่ธาตุตัวหลังต้องระบุจำนวนอะตอมแม้มีเพียงอะตอมเดียว
ตัวอย่างการเรียกชื่อสารประกอบโคเวเลนต์ตัวอย่างการเรียกชื่อสารประกอบโคเวเลนต์ AsF5 อ่านว่า อาร์ซีนิกเพนตะฟลูออไรด์ AlI3อ่านว่า อะลูมิเนียมไตรไอโอไดด์ N2O อ่านว่า ไดไนโตรเจนโมโนออกไซด์ Cl2O7อ่านว่า ไดคลอรีนเฮปตะออกไซด์ CO อ่านว่า คาร์บอนโมโนออกไซด์
ความยาวพันธะ หมายถึง ระยะทางระหว่างนิวเคลียสของอะตอมสองอะตอมที่สร้างพันธะกันในโมเลกุล อะตอมแต่ละชนิดอาจเกิดพันธะมากกว่า 1 ชนิด เช่น C กับ C , N กับ N และพันธะแต่ละชนิดจะมีพลังงานพันธะและความยาวพันธะแตกต่างกัน พันธะเดี่ยว > พันธะคู่ > พันธะสาม
พลังงานพันธะ หมายถึง พลังงานที่ใช้ไปเพื่อสลายพันธะระหว่างอะตอมภายในโมเลกุลซึ่งอยู่ในสถานะแก๊สให้แยกออกเป็นอะตอมในสถานะแก๊ส พลังงานพันธะใช้บอกความแข็งแรงของพันธะ พันธะสาม > พันธะคู่ > พันธะเดี่ยว
CH4 (g) + 423 kJ CH3(g) + H (g) CH3 (g) + 368 kJ CH2(g) + H (g) CH2 (g) + 519 kJ CH (g) + H (g) CH (g) + 335 kJ C (g) + H (g) การสลายพันธะชนิดเดียวกันในโมเลกุลที่มีหลายพันธะ ต้องมีการสลายพันธะหลายขั้นตอน แต่ละขั้นตอนใช้พลังงานไม่เท่ากัน ดังนั้นพลังงานพันธะจึงใช้ค่าเฉลี่ยแทน เรียกว่า พลังงานพันธะเฉลี่ย
พลังงานพันธะเฉลี่ย (Average Bond Energy) พลังงานพันธะเฉลี่ย เป็นค่าเฉลี่ยของพลังงานสลายพันธะสำหรับพันธะแต่ละชนิดในโมเลกุลต่าง ๆ (เป็นค่าโดยประมาณ)
พลังงานพันธะรวมของสารตั้งต้นพลังงานพันธะรวมของสารตั้งต้น พลังงานพันธะรวมของผลิตภัณฑ์ ความร้อนของปฏิกิริยา (Heat of Reaction) การเกิดปฏิกิริยาเคมี คือกระบวนการที่มีการทำลายพันธะเดิม(สารตั้งต้น) และสร้างพันธะใหม่(สารผลิตภัณฑ์) ความร้อนของปฏิกิริยา (Hrxn) คือพลังงานเอนทาลปีของระบบที่เปลี่ยนแปลงไปในรูปความร้อนเมื่อเกิดปฏิกิริยา สามารถหาได้จาก • DHrxnเป็นลบ ปฏิกิริยาคายพลังงาน • DHrxnเป็นบวก ต้องใช้พลังงานเพื่อให้เกิดปฏิกิริยา (ดูดพลังงาน)
การคำนวณหาค่าความร้อนของปฏิกิริยาการคำนวณหาค่าความร้อนของปฏิกิริยา ตัวอย่างจงหาพลังงานที่เปลี่ยนแปลงของปฏิกิริยาต่อไปนี้ CH4(g) + Cl2(g) CH3Cl(g) + HCl(g) • (พลังงานพันธะสารตั้งต้น)= 4D(C-H) + D(Cl-Cl) • (พลังงานพันธะผลิตภัณฑ์ )= D(C-Cl) + 3D(C-H) + D(Cl-H) • Hrxn= 4D(C-H) + D(Cl-Cl)–[D(C-Cl) + 3D(C-H) + D(Cl-H)] = (4414 + 243) –(339 + 3414 + 431) kJ/mol =–113 kJ/mol ปฏิกิริยานี้จะคายความร้อนออกมา 113 kJ/mol
การคำนวณ ตัวอย่างที่ 1 กำหนดพลังงานให้ดังนี้ H – H = 436 kJ/mol N N = 945 kJ/mol และ N – H = 391kJ/mol ปฏิกิริยาเคมีต่อไปนี้ดูดหรือคายพลังงานเท่าใด 2NH3(g) N2 (g) + 3H2 (g)
2NH3(g) N2 (g) + 3H2 (g) 2H – N – H N N + 3(H – H) 6(N – H) N N + 3(H – H) 6 x 391 945 + 3 x 436 2346 kJ 2253 kJ H ปฏิกิริยาดูดพลังงาน = 2346 – 2253 = 93 kJ
รูปร่างโมเลกุล ทำไมต้องศึกษารูปร่างโมเลกุล เพราะสารต่างๆ แม้ว่าจะมีสูตรโมเลกุลเหมือนกันหรือไม่ก็ตามถ้ามีรูปร่างโมเลกุลต่างกัน สมบัติของสารก็แตกต่างกันด้วย รูปร่างของโมเลกุล (รูปทรงทางเรขาคณิต) เกิดจากการจัดตัวของอะตอมภายในโมเลกุลมีผลต่อคุณสมบัติทางกายภาพ (m.p., b.p., density) และเคมี
H O H H H C C C C H H H H H H O H H ตัวอย่างเช่น เอทานอล และ เมทอกซีมีเทน CH3OCH3 CH3CH2OH สมบัติ : ของเหลวไม่มีสี ละลายน้ำได้ดี mp.-117 0C bp. 78.5 0C สมบัติ : แก๊ส ไม่มีสี ไม่ละลายน้ำmp. -138.5 0C bp. -23 0C
จำนวนอะตอมในโมเลกุล จำนวนอิเล็กตรอนคู่ร่วมพันธะ จำนวนอิเล็กตรอนคู่โดดเดี่ยว มุมระหว่างพันธะและความยาวพันธะ ปัจจัยที่มีผลต่อรูปร่างโมเลกุล
106.0 104.0 มุมพันธะ มุมพันธะคือมุมที่เกิดขึ้น เมื่อลากเส้นผ่านพันธะ 2 พันธะมาตัดที่นิวเคลียสของอะตอมกลาง • โมเลกุลที่มีสูตรเคมีคล้ายกัน มุมพันธะอาจไม่เท่ากัน • H2O = 104.5 H2S = 92 • การทำนายโครงสร้างของโมเลกุลเช่น มุมพันธะ จำเป็นต้องอาศัยข้อมูลเกี่ยวกับอิเล็กตรอนในโมเลกุล
A B B O O มุมระหว่างพันธะ (Bond angle) คือ มุมที่เกิดจากอะตอมสองอะตอมทำกับอะตอมกลางหรือมุมที่เกิดระหว่างพันธะสองพันธะ มุม เป็นมุมระหว่างพันธะของโมเลกุล AB2 ซึ่งจะแคบหรือกว้างขึ้นอยู่กับแรงผลักระหว่าง Bond Pair Electron และ Lone PairElectron
การทำนายรูปร่างโมเลกุลการทำนายรูปร่างโมเลกุล พิจารณารูปร่างโมเลกุลจาก Valence Shell Electron Pair Repulsion Model (VSEPR) โดยยึดหลักที่ว่า valence electron pair รอบอะตอมจะมีการผลักกันทำให้อิเล็กตรอนแต่ละคู่อยู่ห่างกัน
โมเลกุลที่อะตอมกลางไม่มี อิเล็กตรอนคู่โดดเดี่ยว 1. โมเลกุลเป็นเส้นตรง (Linear) : AX2 อะตอมกลางมีอิเล็กตรอนคู่ร่วมพันธะ 2 คู่ แต่ละคู่ผลักกันเพื่อให้ห่างกันมากที่สุด เป็นมุมระหว่างพันธะเท่ากับ 180 oC เช่น BeCl2 HCN CO2 C2H2
2. โมเลกุลเป็นรูปสามเหลี่ยมแบนราบ(Trigonal planar) : AX3 อะตอมกลางมีอิเล็กตรอนคู่ร่วมพันธะ 3 คู่ แต่ละคู่ผลักกันห่างกันมากที่สุด เป็นมุมระหว่างพันธะเท่ากับ 120 oC เช่น BF3 SO3 NO3-