ELECTROFORESIS
ELECTROFORESIS. Lic. Julio Roberto Juárez Pernillo quimionauta@gmail.com http://www.quimionauta.blogspot.com Departamento de Fisicoquímica Primer Semestre 2010. ELECTROFORESIS.

ELECTROFORESIS
E N D
Presentation Transcript
ELECTROFORESIS Lic. Julio Roberto Juárez Pernillo quimionauta@gmail.com http://www.quimionauta.blogspot.com Departamento de Fisicoquímica Primer Semestre 2010
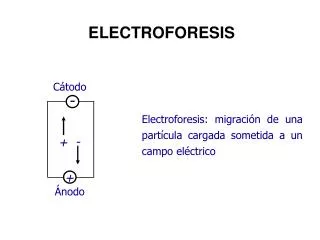
ELECTROFORESIS DEFINICION: Es un método de separación basado en la diferencia de velocidades de migración de especies cargadas eléctricamente en una disolución amortiguadora a la que se aplica un campo eléctrico constante. Desarrollada por Arne Tiselius para el estudio de proteinas séricas (Nobel 1948). Se ha hecho de uso extensivo en biociencias. Solamente la electroforesis tiene la resolución necesaria para distinguir polinucleótidos que difieren en 200 y 500 UMAs en secuenciación de ADN.
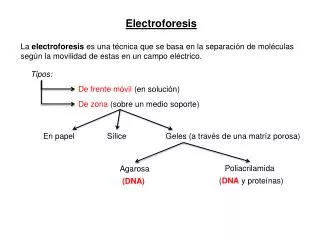
ELECTROFORESIS • TIPOS: Existen dos tipos principales de electroforesis: • Electroforesis convencional. • Electroforesis capilar. • ELECTROFORESIS CONVENCIONAL: Se lleva a cabo sobre una capa delgada y plana o placa de un gel semisólido y poroso que contiene un amortiguador acuoso. Igual que en CCF, se pueden efectuar múltiples separaciones. Las muestras se disponen como manchas o bandas sobre la placa y se aplica un potencial de corriente contínua durante un periodo de tiempo fijo. Las especies separadas se tiñen para visualizarse. Los volúmenes separados son del orden de los μL.
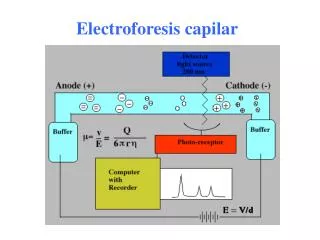
ELECTROFORESIS CAPILAR ELECTROFORESIS CAPILAR: Método instrumental fundamentado en la electroforesis convencional. Relativamente nueva. Da lugar a separaciones de volumenes muy pequeños (de 0.1 a 10 nL), con mucha rapidez y resolución. Usa los mismos detectores cuantitativos que la técnica HPLC, en lugar de las tinciones de la técnica convencional. La velocidad de migración (v), de un ion en cm/s viene dada por: donde E es la intensidad del campo eléctrico (V/cm) y μe es la movilidad electroforética (cm2/V s). E = V/L, donde V es el potencial aplicado en voltios y L es la longitud sobre la que se aplica el campo.
ELECTROFORESIS CAPILAR NUMERO DE PLATOS EN ELECTROFORESIS CAPILAR: Por existir una única fase en la separación, N sólo depende de la difusión longitudinal, y su expresión viene dada por: donde D es el coeficiente de difusión del soluto en cm2/s. Se usan potenciales elevados para mejorar la eficiencia de separación.
Ventajas de la electroforesis capilar • Alta resolución (105a 106platos teóricos)-HPCE • Requiere pequeño volumen de muestra (1-10 nl) • Rápida separación (1 a 45 min.) • Aplicable a todo tipo de sustancias • Automatización • Cuantificación (lineal) • Reproducibilidad • Puede acoplarse a espectrometría de masa • Datos fundamentales
Tipos de moléculas que pueden ser separadas por CE • Proteínas • Péptidos • Amino ácidos • Ácidos nucleicos • Ionesinorgánicos • Bases orgánicas • Ácidos orgánicos
Condiciones de CE • Se utilizan altos voltajes 10-30kV.(>500V/cm; 10-20 mA) • Moléculas positivas, negativas o neutras puede separarse. • La separación se realiza en un tubo capilar de sílica fundida cubierta con poliamida para darle flexibilidad. • El tubo capilar tiene 30-100cm. De longitud y 25-100m de diámetro interno. • Los grupos hidroxilos de la sílica se disocian dejando el tubo con una carga negativa.
ELECTROFORESIS CAPILAR FLUJO ELECTROOSMÓTICO: Movimiento por el cual el disolvente tamponado migra hacia el ánodo o hacia el cátodo. El movimiento es causado por la doble capa eléctrica que se forma en la interfase sílice/disolución. A pH mayor a 3, la pared interna de un capilar de sílice tiene carga negativa por la ionización de los grupos silanol de la superficie. Los cationes del buffer se agrupan sobre la superficie negativa del capilar para formar la doble capa eléctrica. Los cationes situados en la capa exterior difusa de la doble capa son atraidos hacia el cátodo negativo y como están solvatados, arrastran al resto de la disolución con ellos.
Movilidad en CE m = v/E = Q/ 6prh