Tabla de diagonales
Tabla de diagonales. Numero cuántico principal (n).

Tabla de diagonales
E N D
Presentation Transcript
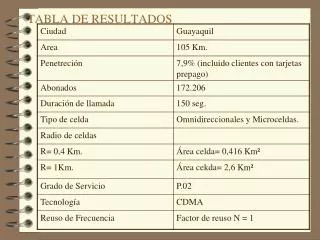
Tabla de diagonales Numero cuántico principal (n). Regla de las Diagonales, debida al científico mexicano Jaime Keller Torres (1936 - ), quien la propuso en 1955. Dicha regla consiste en lo siguiente, se ordenan los orbitales en columna en orden creciente de número cuántico principal n y en renglón en orden creciente de número cuántico azimutal l. Enseguida se trazan líneas diagonales de arriba hacia abajo y de derecha a izquierda que determinan el orden de energía de los orbitales Numero cuántico secundario (azimutal) s,p,d,f.
Los números cuánticos son : n: principal l: (ele) secundariom: magnético s: spin o giro del electrón. En la tabla de diagonales observamos: n y l (ele ) a los valores de ele los llamamos orbitales ó subniveles.
El número cuántico secundario (ele) no describe la forma en que se desplaza el electrón. Sus valores son: Las formas del desplazamiento son:
El numero cuántico magnético: describe la orientación de la forma de la trayectoria.Sus valores son : menos ele a mas ele pasando por cero. La forma l (ele) tiene tres orientaciones en un plano cartesiano y son : x , y , z. La forma s (de esfera no tiene orientación ) por eso aquí el numero magnético ( m ) vale cero
El numero cuántico espín fue introducido en 1925 por Ralph Kronig e, independientemente, por George Uhlenbeck y Samuel Goudsmit. En 1920, los químicos analíticos llegaron a la conclusión que, para describir a los electrones en el átomo, además de los números cuánticos, se requería de un cuarto concepto, el llamado espín del electrón. Éste, al girar sobre su propio eje genera un campo magnético, el denominado espín.
CONCLUSION.Los números cuánticos son: Spin (s) 2 P Secundario (l) Principal (n) x Magnético (m)