Atomy, molekuly
Atomy, molekuly. Částice. Látky. Prvky Sloučeniny. Chemický prvek chemická látka složená z atomů se stejným protonovým číslem Chemická sloučenina chemická látka složená ze dvou nebo více sloučených atomů složená ze stejných molekul. Atom. atom je základní stavební jednotka hmoty


Atomy, molekuly
E N D
Presentation Transcript
Atomy, molekuly Částice
PrvkySloučeniny • Chemický prvek • chemická látka složená z atomů se stejným protonovým číslem • Chemická sloučenina • chemická látka složená ze dvou nebo více sloučených atomů • složená ze stejných molekul
Atom • atom je základní stavební jednotka hmoty • části atomu: • jádro • obal • částice atomu: • v jádře jsou částice: • protony p+kladný náboj • neutrony n0 neutrální náboj • v obale: • elektrony e- záporný náboj
Elektronový obal • v obalu atomu se nachází částice – elektrony • e- mají nepatrnou hmotnost • e- jsou v atomech uspořádány ve vrstvách,slupkách – 1 až 7 slupek • valenční vrstva – poslední, obsahuje valenční elektrony
Atom = prvek • atom je elektroneutrální • obsahuje stejný počet protonů a elektronů • počet protonů v jádře atomu vyjadřuje protonové čísloZ • Celkový počet částic v jádře atomuvyjadřuje nukleonové čísloA http://www.zschemie.euweb.cz/atomy/izotopy.gif
Prvek = atom • každý chemický prvek je určen: • protonovým číslem Z • českým názvem • latinským názvem • chemickou značkou
Názvy prvků vznikly: • podle vlastností prvku • chlor od řeckého chloros – žlutozelený • brom od řeckého bromos - zapáchající • podle toho, odkud byl prvek získán • vápník získán z vápence • vodík z vody • podle země objevu, kde žili objevitelé • germanium – podle Německa • polonium – podle Polska • podle významného chemika • Nobelium – Alfred Bernhard NOBEL • Einsteinium – Albert EINSTEIN
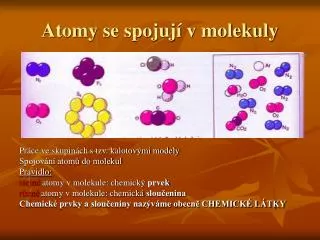
Atomy se slučují do molekul • chemické látky jsou složeny z atomů • málo látek obsahuje jen jednotlivé, nesloučené atomy • helium, argon ve vzduchu He, Ar • většina látek je složena ze spojených atomů – molekul • vlastnost atomů – slučivost • atomy prvků jsou k sobě v molekule poutány chemickými vazbami • slučování atomů stejných prvků (plyny, halogeny) H2 N2 O2 O3 Cl2 F2 , • slučování atomů různých prvků H2O, CO2, NH3, H2SO4 …
Valenční elektrony • jsou v poslední vrstvě atomového obalu • mají největší energii • účastní se chemických reakcí • tvoří vazby mezi atomy - chemické vazby • chemická vazba je tvořena elektronovým párem
Vazebný elektronový pár • atom vodíku má ve valenční vrstvě 1 elektron – nespárovaný • dobře se slučuje s ostatními atomy, které mají také 1 nespárovaný val e • takovým atomem může být další atom vodíku • vzniká dvouatomová molekula H2 H + H →H2 +→ obr. 3 obr. 1 obr. 2 obr. 4
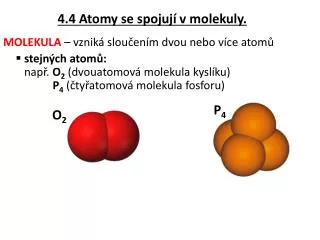
Vznik molekul - chemické prvky • Molekula je částice složená ze dvou nebo více sloučených atomů • 1) sloučením atomů stejného prvku vodík H2 chlór Cl2kyslík O2síra S8ozon O3 Obr. 5 obr. 6 obr. 7 obr. 8 obr.9
Vznik molekul- chemické sloučeniny • Molekula je částice složená ze dvou nebo více sloučených atomů • 2) sloučením atomů dvou nebo více různých prvků vodakyselina sírováoxiduhelnatý DNA H2OH2SO4 CO obr. 10 obr. 11 obr. 12 obr. 13
Chemická sloučenina • Chemické sloučeniny: chemické látky sloučené z atomů různých prvků H + Cl → HCl kyselina chlorovodíková
Popiš kolik prvků a kolik atomů molekula obsahuje prvky atomy
Zdroje: • Obr. 1 http://data.scienceworld.cz/img/article_title/title_l/1c/7111860ee94c82c89ba57930e07d85.jpg • Obr. 2 http://www.zschemie.euweb.cz/atomy/atomh.gif • Obr. 3 http://www.zschemie.euweb.cz/molekuly/molekulah2.gif • Obr. 4 http://t0.gstatic.com/images?q=tbn:ANd9GcTahq0p0BgpKWC5RQSrg-6hJvtFCs9nY7_udgr9Q5Dr7Bmyi64tGA • Obr. 5 http://mail.zsebenese.opava.cz/tabulka/h_0.jpg vodík • Obr. 6 http://upload.wikimedia.org/wikipedia/commons/8/87/Chlorine-3D-vdW.png chlór • Obr. 7 http://www.nyu.edu/pages/mathmol/textbook/oxygen.gif kyslík • Obr. 8 http://upload.wikimedia.org/wikipedia/commons/thumb/b/b9/Ozone-3D-space-filling.png/200px-Ozone-3D-space-filling.png ozón • Obr. 9 http://www.zschemie.euweb.cz/molekuly/s8.gif síra • Obr.10 http://chemiesychrov.sweb.cz/molekulaH2O.png • Obr. 11 http://oko.yin.cz/1/kyselina-sirova/kyselina-sirova.jpg • Obr.12 http://upload.wikimedia.org/wikipedia/commons/thumb/a/a7/Carbon-monoxide-3D-vdW.png/135px-Carbon-monoxide-3D-vdW.png • Obr. 13 http://www.biology.arizona.edu/home/DNA.gif • Obr.14 http://www.vyukovematerialy.cz/chemie/rocnik8/foto/polvaz.gif