TERMODINAMIKA
TERMODINAMIKA. Kelompok 9 Kholil Aziz Hasri K3311043 Mustika Dewi I K3311055 Rahardian P K3311064 Rose Oriza K3311072 Arip Budhi H K3308070. Pengertian Termodinamika.


TERMODINAMIKA
E N D
Presentation Transcript
TERMODINAMIKA Kelompok 9 Kholil Aziz Hasri K3311043 Mustika Dewi I K3311055 Rahardian P K3311064 Rose Oriza K3311072 Arip Budhi H K3308070
Pengertian Termodinamika Termodinamikaadalahilmutentangenergi, yang secaraspesifikmembahastentanghubunganantaraenergi(U, H, S, G, A), panas (q)dengankerja (w). Berasaldaridua kata Yunaniyaituthermos (heat) dan dynamis (power). Ataudengan kata lainThermodinamika adalah ilmu yang membahas hubungan antara panas dengan kerja.
Dalam thermodinamika, besaran sistem dapat dibagi menjadi dua besaran thermodinamika yaitu : besaran Extensive dan besaran Intensive. Besaran extensive dipengaruhi oleh massa atau mole sistem, sedangkan besaran intensive tidak dipengaruhi oleh massa atau mole sistem sistem. Contoh : Besaran extensive : Volume, Kapasitas Panas, Kerja (energi), entropy dll. Besaran intensive : Tekanan, Temperatur, kerapatan dll.
MengapaperubahanTerjadi ? Prosesspontan Berlangsungdengansendirinya “secaraalami” tanpamemerlukanpemicu Prosestidakspontan Diperlukansesuatuuntukbisaberlangsung
Sistem Sistemadalahsuatu massa atau daerah yang dipilih, untukdijadikanobyekanalisis. • Lingkungan Lingkunganadalahsegalasesuatu yang beradadiluarsistem. • Batas Sistem Batas sistemadalahbatas antara sistem dengan lingkungannya. Dalamaplikasinyabatassistemmerupakanbagiandarisistemmaupunlingkungannya, dandapattetapataudapatberubahposisiataubergerak.
PengertianSistem Sistemadalahsuatu massa atau daerah yang dipilih, untukdijadikanobyekanalisis. Atausistemadalahsegalasesuatu yang ingindipelajari. SistemTermodinamikaadatigamacam, yaitu : • Sistemtertutup Dalamsistemtertutupmassadarisistem yang dianalisistetapdantidakadamassakeluardarisistemataumasukkedalamsistem,tetapivolumenyabisaberubah. Yang dapatkeluarmasuksistemtertutupadalahenergidalambentukpanasataukerja. Ataudengankata lain sistemtertutupberisimateri yang sama, dimanaperpindahanmassamelaluibatassistemtidakdimungkinkan. Contohsistemtertutupadalahsuatubalonudara yang dipanaskan, dimanamassaudaradidalambalontetap, tetapivolumenyaberubah, danenergipanasmasuk kedalam massa udara didalam balon.
Sistemterbuka Dalamsistemterbuka, energidanmasadapatkeluarsistemataumasukkedalamsistemmelewatibatassistem. Sebagianbesarmesin-mesinkonversi energi adalah sistem terbuka. Sistem mesin motor bakar adalahruangdidalamsilindermesin, dimanacampuranbahanbahanbakardanudaramasukkedalamsilinder, dan gas buangkeluarsistemmelaluiknalpot. Turbin gas, turbinuap, pesawat jet dan lain-lain adalahmerupakan sistem termodinamika terbuka, karena secara simultan ada energidanmassakeluar-masuksistemtersebut. • Sistemterisolasi Tidakadapertukaranmassadanenergisistemdenganlingkungan. Ataudengankata lain sistemtidakterpengaruhsamasekaliolehlingkungan Misalnya: Tabung gas yang terisolasi.
Redistribusipartikel gas dalamwadahterjaditanpaperubahanenergidalam total sistem, semuasusunanekivalen • Jumlahcarakomponensistemdapatdisusuntanpamerubahenergisistemterkaiteratdengankuantitasentropi (S) • Entropiadalahukuranketidakteraturansistem • Sistemdengancaratersusunekivalenkomponennyasedikitsepertikristalpadatmemilikiketidakteraturan yang kecilatauentropirendah • Sistemdengancaratersusunekivalenkomponennyabanyakseperti gas memilikiketidakteraturanbesaratauentropitinggi
Jikaentropisistemmeningkat, komponensistemmenjadisemakintidakteratur, random danenergisistemlebihterdistribusipada range lebihbesarSdisorder > Sorder • Sepertihalnyaenergidalamatauentalpi, entropijugafungsikeadaanyaituhanyatergantungpadakeadaanawaldanakhirtidakpadabagaimanaprosesterjadinya Ssis = Sfinal – Sinitial • Jikaentropimeningkatmaka Ssisakanpositif, sebaliknyajikaentropiturun, maka Ssisakannegatif
Macam-macam hukum Termodinamika • Hukum Awal (Zeroth Law) Termodinamika • Hukum Pertama Termodinamika • Hukum Kedua Termodinamika • Hukum ketiga termodinamika
A B C • HukumTermodinamikakeNol • Hukum inimeletakkkankonsepsuhu padadasar yang kokoh, yaitubiladuasistemadadalamkesetimbangantermal, makakeduanyamempunyaisuhu yang sama, bilatakadadalamkesetimbangantermalmakakeduanyamempunyaisuhu yang berbeda. • Tinjau 3 sistem A, B dan C, Faktaeksperimental : bilasistem A adadalamkesetimbangantermaldengansistem B, dansistem B jugaadadalamkesetimbangantermaldengan C maka A adadalamkesetimbangandengan C: - TA = TB TA = TC - TB = TC
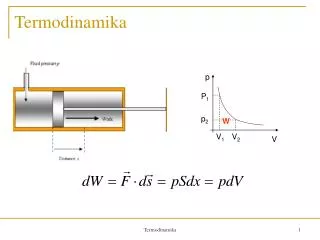
HukumTermodinamikaPertama • Jika suatu benda dipanaskan yang berarti diberi kalor Q, benda akan mengembang atau bertambah volumenya yang berarti melakukan usaha W dan benda akan bertambah panas yang berarti mengalami perubahan energi dalam ∆U. • Secaramatematis. hukumtermodinamika I padasistemtertutup, dinyatakansebagai: dU = dq + dw U = q + w • Dengankata lain, perubahanenergidalamsistem (U) setaradenganpanas yang diberikanpadasistem (q) dankerja yang dilakukanterhadapsistem (w) • Jikahanyadiberikanpanas, berlaku: U = q • Jikahanyadilakukankerjaberlaku: U = w
HukumTermodinamikaKedua Dalam setiap perubahan yang sepontan selalu diikuti kenaikan entropi dalam alam semesta ini Contoh:penurunan entropi pada pembangunan dinding bata dari suatu tumpukan batu bata,tetapi pasti ada hal lain yang terjadi yang menghasilkan kenaikan entropi yang lebih besar yaitu kegiatan orang yang membuat dinding tersebut
HukumTermodinamikaKetiga • Pada suhu nol absolut,entropi dari kristal zat yang murni adalah nol
Sekian & Terima Kasih Any question ?