Real-Time PCR
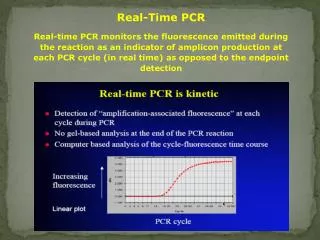
Real-Time PCR Real-time PCR monitors the fluorescence emitted during the reaction as an indicator of amplicon production at each PCR cycle (in real time) as opposed to the endpoint detection. Kvatitativní PCR v reálném čase


Real-Time PCR
E N D
Presentation Transcript
Real-Time PCR Real-time PCR monitors the fluorescence emitted during the reaction as an indicator of amplicon production at each PCR cycle (in real time) as opposed to the endpoint detection
Kvatitativní PCR v reálném čase Tato technika je založena na použití fluorescenčně značených sond a detekčního systému, který je schopen měřit intenzitu fluorescence. Intenzita fluorescence je tak uměrná množství PCR produktu a pomocí kalibrační křivky sestrojené za použití známých množství cílové DNA je možné přesně kvantifikovat množství cílové DNA v biologickém vzorku. Princip metody Oligonukleotidová sonda označená dvěma fluorochromy nasedá na cílovou sekvenci uvnitř amplifikovaného PCR produktu. Fluorochrom na 5´konci je označován jako reportér a fluorochrom na 3´ konci jako zhášeč. Jestliže jsou oba fluochromy přítomny na jedné DNA molekule, nedochází k žádnému vyzařování fluorescence. V okamžiku, kdy Taqpolymerasazahají další kolo syntézy, dochází díky její exonukleasové aktivitě k degradaci sondy a reportérovýfluorochrom je uvolněn ze zhasnutého stavu. Intenzita fluorescence je monitorována kontiuálně během amplifikačního procesu, vždy na konci jednotlivých cyklů. Intenzita fluorecence tedy přímo odpovídá množství PCR produktu v reakci. PCR v reálném čase je poměrné nenáročná na provedení a je vysoce reprodukovatelná. Další výhodou je možnost analyzovat velké množství vzorků najednou. Hlavním limitem této metody zatím však zůstává vysoká pořizovací cena potředných zařízení V tomto případě odpovídá fluorescence z uvolněných fluoroforů počtu dokončených kopií amplifikované DNA. Toto uspořádání se označuje jako tzv. Taq Man analýza. Je nutné podotknout, že byla vyvinuta řada dalších principů sledování intenzit fluorescence v průběhu PCR. Za zmínku stojí třeba v současné době nejpokročilejší přístup s univezálnímiprimeryAmplifluor, které vytvářejí intramolekulární vlásenku a jsou označeny na jednom konci fluoroforem a uprostřed před začátkem prodloužení zhášečem. Tímto přístupem bylo dosaženo určitého zlevnění oproti předcházejícím systémům, protože se nevyžaduje chemická syntéza pro každý případ nového, fluorescenčně značeného primeru.
Real-time PCR advantages * not influenced by non-specific amplification * amplification can be monitored real-time * no post-PCR processing of products (high throughput, low contamination risk) * ultra-rapid cycling (30 minutes to 2 hours) * wider dynamic range of up to 1010-fold * confirmation of specific amplification by melting point analysis * most specific, sensitive and reproducible * not much more expensive than conventional PCR (except equipment cost)
Real-time PCR disadvantages * not ideal for multiplexing * setting up requires high technical skill and support * high equipment cost * * * * intra- and inter-assay variation * RNA lability * DNA contamination (in mRNA analysis)
Real-time Principles • based on the detection and quantitation of a fluorescent reporter • Three general methods for the quantitative detection: • 1. Hydrolysis probes(TaqMan, Beacons) • 2. Hybridisation probes(Light Cycler) • 3. DNA-binding agents(SYBR Green)
Principles of Real-Time Quantitative PCR techniques • SYBR Green I technique: SYBR Green I fluorescence is enormously increased upon binding to double-stranded DNA. During the extension phase, more and more SYBR Green I will bind to the PCR product, resulting in an increased fluorescence. Consequently, during each subsequent PCR cycle more fluorescence signal will be detected. • Hydrolysis probe technique: The hydrolysis probe is conjugated with a quencher fluorochrome, which absorbs the fluorescence of the reporter fluorochrome as long as the probe is intact. However, upon amplification of the target sequence, the hydrolysis probe is displaced and subsequently hydrolyzed by the Taq polymerase. This results in the separation of the reporter and quencher fluorochrome and consequently the fluorescence of the reporter fluorochrome becomes detectable. During each consecutive PCR cycle this fluorescence will further increase because of the progressive and exponential accumulation of free reporter fluorochromes. • Hybridisation probes technique: In this technique one probe is labelled with a donor fluorochrome at the 3’ end and a second –adjacent- probe is labelled with an acceptor fluorochrome. When the two fluorochromes are in close vicinity (1–5 nucleotides apart), the emitted light of the donor fluorochrome will excite the acceptor fluorochrome (FRET). This results in the emission of fluorescence, which subsequently can be detected during the annealing phase and first part of the extension phase of the PCR reaction. After each subsequent PCR cycle more hybridisation probes can anneal, resulting in higher fluorescence signals.
SYBR Green I technique:SYBR Green I fluorescence is enormously increased upon binding to double-stranded DNA. During the extension phase, more and more SYBR Green I will bind to the PCR product, resulting in an increased fluorescence. Consequently, during each subsequent PCR cycle more fluorescence signal will be detected.
Hydrolysis probe technique:The hydrolysis probe is conjugated with a quencher fluorochrome, which absorbs the fluorescence of the reporter fluorochrome as long as the probe is intact. However, upon amplification of the target sequence, the hydrolysis probe is displaced and subsequently hydrolyzed by the Taq polymerase. This results in the separation of the reporter and quencher fluorochrome and consequently the fluorescence of the reporter fluorochrome becomes detectable. During each consecutive PCR cycle this fluorescence will further increase because of the progressive and exponential accumulation of free reporter fluorochromes.
Taq man DNA Polymerase 5' exonuclease activity
Hybridisation probes technique:In this technique one probe is labelled with a donor fluorochrome at the 3’ end and a second –adjacent- probe is labelled with an acceptor fluorochrome. When the two fluorochromes are in close vicinity (1–5 nucleotides apart), the emitted light of the donor fluorochrome will excite the acceptor fluorochrome (FRET). This results in the emission of fluorescence, which subsequently can be detected during the annealing phase and first part of the extension phase of the PCR reaction. After each subsequent PCR cycle more hybridisation probes can anneal, resulting in higher fluorescence signals.
What is CT? The Amplification Plot contains valuable information for the quantitative measurement of DNA or RNA. The Threshold line is the level of detection or the point at which a reaction reaches a fluorescent intensity above background. The threshold line is set in the exponential phase of the amplification for the most accurate reading. The cycle at which the sample reaches this level is called the Cycle Threshold, CT. These two values are very important for data analysis using the 5’ nuclease assay.
Albumin (ALB) gene dosage by real-time PCR Laurendeau et al. Clin Chem 1999(www)
What is DRn? +Rn Sample Rn Threshold Rn -Rn No Template Control CT 0 10 20 30 40 cycle number
Praktické uplatnění metody Spektrum aplikací kvantitativní PCR v reálném čase je podobné jako pro nekvantitativní techniky. Obrovskou výhodou je informace o kvantitě detekovaného produktu. To je klíčové pro kvantifikaci fytopatogenního organismu v analyzovaném vzorku. Znalost množství infekčního agens dovoluje v dostatečném předstihu volit konkrétní přímé metody ochrany rostlin nebo fytokaranténní opatření. Boyleetal. (2005) za použití kvantitivní PCR v reálném čase studovali dynamiku růstu fytopatogenních hub rodu Melampsora. Na základě kvantifikace DNA těchto fytopatogenů v jednotlivých stádií růstu, od inokulace až po tvoru urédií, se jim podařilo sestrojit růstové křivky pro jednotlivé druhy rodu Melapsora. Stejně tak byli úspěšní při monitorování výskytu těchto hub před objevením prvních pozorovatelných příznaků choroby, čímž byly potvrzeny i prakticky možnosti této techniky. Jelikož citlivost této techniky mnohonásobně převyšuje klasické imunochemické metody detekce rostlinných virů, jako je např. ELISA, má i zde PCR v reálném čase své uplatnění. Schneider etal. (2004) vyvinuli a optimalisovali metodu kvatitativní PCR detekce fytopatologicky významného viru šárky švestky (angl. plumpox virus) v souvislosti s jeho nedávným prvním výskytem v Kanadě.
LAMP Loop mediated isothermal amplification “LAMP” which stands for Loop-mediated Isothermal Amplification is a simple, rapid, specific and cost-effective nucleic acid amplification method solely developed by Eiken Chemical Co., Ltd. It is characterized by the use of 4 different primers specifically designed to recognize 6 distinct regions on the target gene and the reaction process proceeds at a constant temperature using strand displacement reaction. Amplification and detection of gene can be completed in a single step, by incubating the mixture of samples, primers, DNA polymerase with strand displacement activity and substrates at a constant temperature (about 65°C). It provides high amplification efficiency, with DNA being amplified 109-1010 times in 15-60 minutes. Because of its high specificity, the presence of amplified product can indicate the presence of target gene.