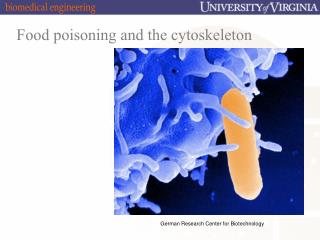
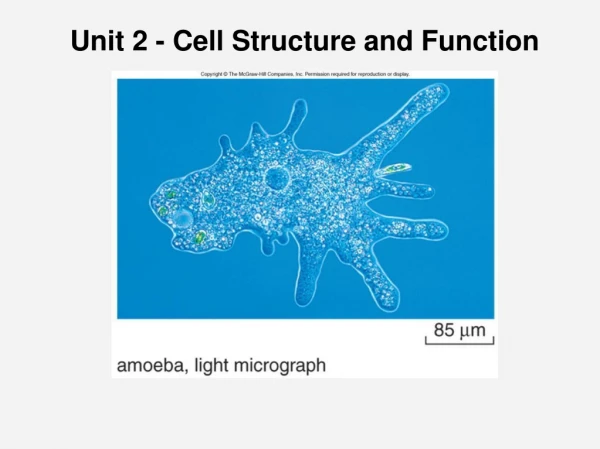
第ä¹ç« 细胞骨架 (Cytoskeleton)
第ä¹ç« 细胞骨架 (Cytoskeleton). 第一节 细胞骨架的概述. â—† 细胞骨架 概念 细胞骨架是指å˜åœ¨äºŽçœŸæ ¸ç»†èƒžçš„细胞质ä¸çš„ 蛋白纤维网架结构体系 â—† 有ç‹ä¹‰å’Œå¹¿ä¹‰ä¸¤ç§æ¶µä¹‰  在细胞质基质ä¸åŒ…括微ä¸ã€å¾®ç®¡å’Œä¸é—´çº¤ç»´ã€‚  åœ¨ç»†èƒžæ ¸ä¸å˜åœ¨æ ¸éª¨æž¶ - æ ¸çº¤å±‚ä½“ç³»ã€‚æ ¸éª¨æž¶ã€ æ ¸çº¤å±‚ä¸Žä¸é—´çº¤ç»´åœ¨ç»“构上相互连接 , 贯穿于 ç»†èƒžæ ¸å’Œç»†èƒžè´¨çš„ç½‘æž¶ä½“ç³»ã€‚. å¾® ä¸ å¾® 管 ä¸é—´çº¤ç»´. ç‹ä¹‰ :. 细胞质骨架. 细胞 骨架. ç»†èƒžæ ¸éª¨æž¶ 细胞质骨架 细胞膜骨架 细胞外基质. 广义. å¾®ä¸ï¼šç¡®å®šç»†èƒžè¡¨é¢çš„特å¾ï¼Œå¹¶ä½¿ç»†èƒžå®Œæˆè¿åŠ¨å’Œæ”¶ç¼©ï¼›

第ä¹ç« 细胞骨架 (Cytoskeleton)
E N D
Presentation Transcript
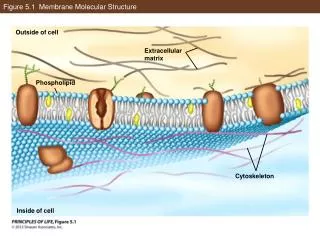
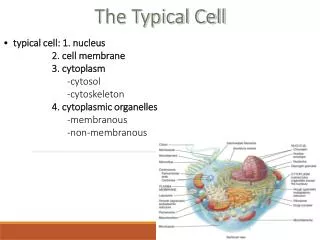
第一节 细胞骨架的概述 ◆细胞骨架概念 细胞骨架是指存在于真核细胞的细胞质中的蛋白纤维网架结构体系 ◆有狭义和广义两种涵义 在细胞质基质中包括微丝、微管和中间纤维。 在细胞核中存在核骨架-核纤层体系。核骨架、 核纤层与中间纤维在结构上相互连接,贯穿于 细胞核和细胞质的网架体系。
微 丝 微 管 中间纤维 狭义: 细胞质骨架 细胞 骨架 细胞核骨架 细胞质骨架 细胞膜骨架 细胞外基质 广义
微丝:确定细胞表面的特征,并使细胞完成运动和收缩;微丝:确定细胞表面的特征,并使细胞完成运动和收缩; • 微管:确定膜性细胞器的位置和作为膜内物质运输的“高速公路”网络; • 中间纤维:赋予细胞张力和抗剪切力
◆细胞骨架主要功能的概述 作为动态的支架,提供结构支撑以决定细胞形状和抵抗细胞变形。 作为在细胞内定位各种细胞器的内部框架。 作为高速公路网指导物质与细胞器在细胞内的运动。 作为产生力的装置,将细胞从一个地方移至到另一个地方,细胞的运动功能的实现都与细胞骨架有关。 作为锚定mRNA并促进其翻译成多肽的位点。 作为细胞分裂的必要组分,细胞骨架成分组成的细胞器负责牵引染色体的分离,并将亲代细胞分成两个子代细胞 。
二、细胞骨架的遗传学方法研究 采用突变的方式来研究细胞骨架蛋白的功能。 (一)过量表达显性失活突变蛋白 显性失活的基因转染→筛选阳性克隆→使突变蛋白过量表达→突变蛋白与正常蛋白(表达量低)竞争→细胞表现出突变蛋白的表型→确定目的蛋白的功能 例:显性失活的驱动蛋白Ⅱ(kinesin Ⅱ)即使在激素刺激下,也是非洲爪蟾不能分泌色素颗粒,说明驱动蛋白Ⅱ负责色素颗粒的运输和分泌。
(二)实验动物的基因敲除 基因敲除技术:使动物缺乏特定的基因,研究特定基因敲除后的效应。有些基因敲除后小鼠可能出现高度特异性的缺陷,说明敲除的基因在缺陷涉及的活动中具有重要的作用。 例:敲除细胞质中动力蛋白(dynein)的小鼠在出生后8天死亡,研究其胚胎细胞发现高尔基体发生断裂,分散在细胞质中,说明动力蛋白是高尔基体在细胞内正确定位的必需分子。
第二节 微丝 又称肌动蛋白纤维(actin filament), 是指真核细胞中由肌动蛋白(actin)组成、直径为7nm的骨架纤维
成 分 ●肌动蛋白(actin) 是微丝的主要结构成分,外观呈哑铃状, 这种actin又叫G-actin,将G-actin形成的微丝又称为F-actin。存在于所有真核细胞中,在真核细胞进化过程中高度保守。在细胞内与几乎所有形式的运动相关。
一、微丝(microfilament, MF) 又称肌动蛋白纤维(actin filament), 是指真核 细胞中由肌动蛋白(actin)组成、直径为7nm的骨架纤维。 ●成分 ●装配 ●微丝结合蛋白 ●微丝特异性药物 ●微丝功能 ●肌肉收缩(muscle contraction)
一、微丝的分子结构 成分:肌动蛋白(actin) 是微丝的主要结构成分,外观呈哑铃状, 这种actin又叫球形肌动蛋白(G-actin),将G-actin形成的多聚体称为纤维形肌动蛋白(F-actin)。存在于所有真核细胞中,在真核细胞进化过程中高度保守.
装 配 ◆ATP-肌动蛋白对微丝纤维末端亲和力高,ADP-肌动蛋白对纤维末端亲和力低,容易脱落 ◆ MF是由G-actin单体形成的多聚体,肌动蛋白单体具有极性, 装配时呈头尾相接, 故微丝具有极性,既正极与负极之别。 ◆ 体外实验表明,MF正极与负极都能生长,生长快的一端为正极,慢的一端为负极;去装配时,负极比正极快。由于G-actin在正极端装配,负极去装配,从而表现为踏车行为。
◆ 两条F-肌动蛋白链螺旋盘绕形成微丝(或1条形成的螺旋链) ◆ 微丝有些是永久性的结构(如肌原纤维、微绒毛等),有些是暂时性的结构,处于动态的装配和解聚过程中。 ◆体内肌动蛋白的装配在两水平受到结合蛋白的调节:1、ATP-肌动蛋白单体的浓度;2、微丝连接成束或成网的程度。
微丝特异性药物 ◆细胞松弛素(cytochalasins):可以切断微丝,并结合在微丝正极阻抑肌动蛋白聚合,因而导致微丝解聚。 ◆鬼笔环肽(philloidin):与微丝侧面结合,防止MF解聚。只与F肌动蛋白结合,不与G肌动蛋白结合。使微丝纤维稳定而抑制其功能 ◆影响微丝装配动态性的药物对细胞都有毒害,说明微丝功能的发挥依赖于微丝与肌动蛋白单体库间的动态平衡。这种动态平衡受actin单体浓度和微丝结合蛋白的影响。
二、微丝结合蛋白 微丝系统=肌动蛋白纤维+微丝结合蛋白。 肌动蛋白纤维的组织和行为需要与微丝结合的其他蛋白的相互作用,这些蛋白可协助完成肌动蛋白纤维的装配和解聚,影响肌动蛋白纤维的相互作用、物理性质以及与其他细胞器的连接功能等。 整个骨架系统结构和功能在很大程度上受到不同的细胞骨架结合蛋白的调节。
(一)成核蛋白 成核现象是纤维装配的第一步,也是最慢的一步。首先2-3个肌动蛋白单体装配成多聚体核心,然后其他单体陆续添加到核心上,形成肌动蛋白纤维。 肌动蛋白相关蛋白复合体分子由Arp2、Arp3和5种其他蛋白构成,与肌动蛋白在结构上具有同源性。该类分子在体内外都可以促进肌动蛋白的成核。
(二)单体隐蔽蛋白 细胞中约有50%的肌动蛋白为可溶性肌动蛋白,大大高于肌动蛋白组装所需的临界浓度。但是这些蛋白与其它蛋白结合,构成一个隐蔽的蛋白库。只有当细胞需要组装纤维的时候这些可溶性肌动蛋白才被释放出来。如:thymosin与actin结合可阻止其向纤维添加,抑制其水解或交换结合的核苷酸。胸腺肽与肌动蛋白结合可阻止其向纤维上装配,与G肌动蛋白结合并维持其单体稳定,蛋白浓度或活性变化可以调整单体-聚合物间的平衡,决定装配或解聚。
(三)封端蛋白 作用是调节肌动蛋白纤维的长度,结合在(+)或(-)极形成“帽子”,阻止其它单体添加。如骨骼肌细肌丝的(-)端被tropomodulin封闭,(+)端被CapZ封闭。
(四)单体聚合蛋白 G-肌动蛋白结合蛋白结合在机动蛋白ATP结合位点的另一侧,能与胸腺肽竞争结合肌动蛋白,G-肌动蛋白结合蛋白可将所结合的单体组装到微丝纤维的(+)端。细胞运动时,G-肌动蛋白结合蛋白可促进肌动蛋白的装配。
(五)微丝解聚蛋白 如cofilin可结合在纤维的(-)极,使微丝去组装。这种蛋白在微管快速组装和去组装的结构中具有重要的作用,涉及细胞的移动、内吞和胞质分裂 (六)交联蛋白 每一种蛋白含有2至多个微丝结合部位,因此可以将2至多条纤维联系在一起形成纤维束或网络。分为成束蛋白和成胶蛋白两类,成束蛋白如:丝束蛋白(fimbrin)、绒毛蛋白(villin)和α-辅肌动蛋白(α-actinin),可以将肌动蛋白纤丝交联成平行排列成束的结构。成胶蛋白,如细丝蛋白(filamin)促使形成肌动蛋白微丝网
(七)纤维切割蛋白 此类蛋白能结合在微丝中部,将微丝切断。如溶胶蛋白(gelsolin)。 (八)膜结合蛋白 非肌肉细胞的收缩部位主要位于质膜下面,膜结合蛋白包括黏着斑蛋白,ERM家族等。黏着斑蛋白可将肌动蛋白纤维连接到膜上,参与构成黏着带。
三、肌肉收缩系统 粗肌丝 肌球蛋白 肌肉 肌原纤维 肌动蛋白 细肌丝 原肌球蛋白 肌钙蛋白
肌肉收缩系统中的有关蛋白 ①肌球蛋白(myosin) 头部具ATP酶活力,沿微丝从负极到正极进行运动。主要分布于肌细胞,有两个球形头部结构域(具有ATPase活性)和尾部链,多个Myosin尾部相互缠绕,形成myosin filament,即粗肌丝。 Myosin II是构成肌纤维的主要成分之一。由两个重链和4个轻链组成,重链形成一个双股α螺旋,一半呈杆状,另一半与轻链一起折叠成两个球形区域,位于分子一端,球形的头部具有ATP酶活性(图9-9)。 Myosin V结构类是于myosin II,但重链有球形尾部。 Myosin I 由一个重链和两个轻链组成。 Myosin I、II、V都存在于非肌细胞中,II型参与形成应力纤维和胞质收缩环,I、V型结合在膜上与膜泡运输有关,神经细胞富含myosin V 。
②原肌球蛋白(tropomyosin, Tm) 原肌球蛋白(tropomyosin.Tm)分子量64KD,是由两条平行的多肽链扭成螺旋,每个Tm的长度相当于7个肌动蛋白,呈长杆状。原肌球蛋白与肌动蛋白结合,位于肌动蛋白双螺旋的沟中,主要作用是加强和稳定肌动蛋白丝,抑制肌动蛋白与肌球蛋白结合
③肌钙蛋白(Troponin, Tn)为复合物,分子量80KD,包括三个亚基:TnC(Ca2+敏感性蛋白) 能特异与Ca2+结合; TnT(与原肌球蛋白结合); TnI(抑制肌球蛋白ATPase活性),细肌丝中每隔40nm就有一个肌钙蛋白复合体
四、肌肉收缩 肌细胞上的动作电位引起肌质网Ca2+电位门通道开启,肌浆中Ca2+浓度升高,肌钙蛋白与Ca2+结合,引发原肌球蛋白构象改变,暴露出肌动蛋白与肌球蛋白的结合位点。肌动蛋白通过结合与水解ATP、不断发生周期性的构象改变、引起粗肌丝和细肌丝的相对滑动。
肌动蛋白的工作原理可概括如下: ①肌球蛋白结合ATP,引起头部与肌动蛋白纤维分离; ②ATP水解,引起头部与肌动蛋白弱结合; ③Pi释放,头部与肌动蛋白强结合,头部向M线方向弯曲(微丝的负极),引起细肌丝向M线移动; ④ADP释放ATP结合上去,头部与肌动蛋白纤维分离。如此循环
四、微丝的功能 1.形成应力纤维(stress fiber):非肌细胞中的应力纤维与肌原纤维有很多类似之处:都包含myosin II、原肌球蛋白、filamin和α-actinin。培养的成纤维细胞中具有丰富的应力纤维,并通过粘着斑固定在基质上。在体内应力纤维使细胞具有抗剪切力
2.形成微绒毛 ; 3.细胞的变形运动: 分为四步: ①:微丝纤维生长,使细胞表面突出,形成片足(lamellipodium); ②在片足与基质接触的位置形成粘着斑; ③在myosin的作用下微丝纤维滑动,使细胞主体前移; ④解除细胞后方的粘和点。如此不断循环,细胞向前移动。阿米巴原虫、白细胞、成纤维细胞都能以这种方式运动。
4.胞质分裂:有丝分裂末期,两个即将分离的子细胞内产生收缩环,收缩环由平行排列的微丝和myosin II组成。随着收缩环的收缩,两个子细胞的胞质分离,在细胞松驰素存在的情况下,不能形成胞质分裂环,因此形成双核细胞。
5.顶体反应:在精卵结合时,微丝使顶体突出穿入卵子的胶质里,融合后受精卵细胞表面积增大,形成微绒毛,微丝参与形成微绒毛,有利于吸收营养。5.顶体反应:在精卵结合时,微丝使顶体突出穿入卵子的胶质里,融合后受精卵细胞表面积增大,形成微绒毛,微丝参与形成微绒毛,有利于吸收营养。
6.其他功能:如细胞器运动、质膜的流动性、胞质环流均与微丝的活动有关,抑制微丝的药物(细胞松弛素)可增强膜的流动、破坏胞质环流。6.其他功能:如细胞器运动、质膜的流动性、胞质环流均与微丝的活动有关,抑制微丝的药物(细胞松弛素)可增强膜的流动、破坏胞质环流。
第三节 微 管(Microtubules) 微管在胞质中形成网络结构,作为运输路轨并起支撑作用。微管是由微管蛋白组成的管状结构,对低温、高压和秋水仙素敏感。
一、微管的分子结构 微管是由13条原纤维(protofilament)构成的中空管状结构,直径22~25nm。每一条原纤维由微管蛋白二聚体线性排列而成。微管蛋白二聚体由结构相似的α和β球蛋白构成,两种亚基均可结合GTP,α球蛋白结合的GTP从不发生水解或交换,是α球蛋白的固有组成部分,β球蛋白结合的GTP可发生水解,结合的GDP可交换为GTP,可见β亚基也是一种 G蛋白