Amino kiselini
Amino kiselini. Proteinite vo organizmot se sostaveni od kombinacija na 20 razli~ni subedinici nare~eni a -amino kiselini. a -AMINO KISELINI. a - jaglerodniot atom na sekoja amino kiselinite e povrzan so: vodoroden atom, karboksilna grupa, amino grupa i


Amino kiselini
E N D
Presentation Transcript
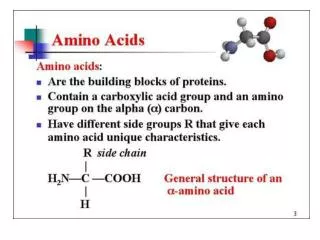
Proteinite vo organizmot se sostaveni od kombinacija na 20 razli~ni subedinici nare~eni a-amino kiselini.
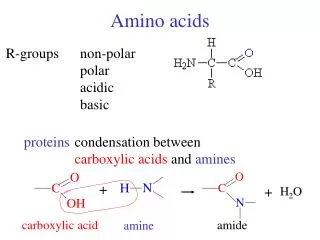
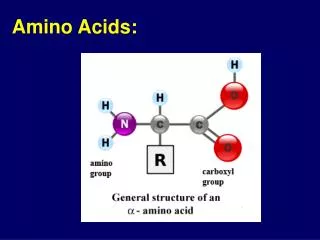
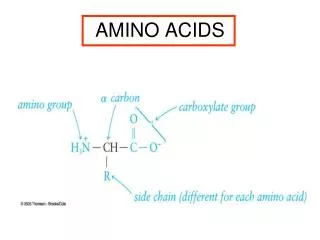
a-AMINO KISELINI a - jaglerodniot atom na sekoja amino kiselinite e povrzan so: • vodoroden atom, • karboksilna grupa, • amino grupa i • strani~en sinxir ili karakteristi~en radikal Zaradi prisustvo na karboksilna i amino grupa kaj site amino kiselini, site razliki me|u niv }e zavisat od nivnie radikalni grupi vo strani~niot sinxir.
Op{ta struktura na edna a-amino kiselina Strani~en sinxir - R grupa
Struktura na prolin, razli~na od site drugi amino kiselini izolirani od proteini Prolin
Konfiguracija na amino kiseliniteLiDizomerija Konfiguracijata se opredeluva spored konfiguracijata na gliceraldehidot
Amino kiselini kako dipolarni joniDisocirani formi na a-amino kiselina
Hemiski reakcii na amino kiselina 1. Reakcii na karboksilnata grupa a) disocijacija na karboksilnata grupa (dobivawe soli) b) dobivawe esteri (vo reakcija so alkoholi) v) dekarboksilacija na amino kiselinite (dobivawe amin) g) redukcija na karboksilnata grupa (dobivawe primaren amino alkohol)
Hemiski reakcii na amino kiselina 2. Reakcii na amino grupata a) reakcija so azotesta kiselina b) boeni reakcii na amino grupata (ninhidrin) v) reakcija so aldehidi (dobivawe na Shif-ovi bazi) g) reakcija so SO2 (karbamino kiselina za prenos na O2) d) reakcija so te{ki metali ( So2+,Cu2+ oboeni kompleksi) |) reakcija so –SOON (peptidna vrska)
Opti~ka aktivnost na amino kiselinite a-S atomot kaj alfa amino kiselinite e hiralen, osven kaj glicinot. * a-aminokiselina Glicin *, hiralen S-atom
Podelba na amino kiselinite Nepolarni, hidrofobni • Strani~nite sinxiri se nepolarni. • Se nao|aat dlaboko vo vnatre{nosta na proteinot • Tamu se povrzuvaat edna so druga i ostanuvaat izolirani od vodata.
Podelba na amino kiselinite Polarni - hidrofilni • strani~nite sinxiri se polarni • privlekuvaat molekuli voda • se nao|aat na povr{inata na proteinite Podeleni se na 3 klasi: - polarni neutralni - negativno naelektrizirani - pozitivno naelektrizirani
Polarni neutralni amino kiselini • radikalnite imaat golem afinitet kon vodata; • pri rN = 7 ne se jonizirani; • se povrzuvaat so druga molekula preku vodorodna vrska; • cisteinskite molekuli formiraat disulfidni vrski so druga molekula;
Negativno naelektriziranimonoamino dikarboksilni kiselini • imaat jonizirani karboksilni grupi vo strani~en sinxir; • pri rN = 7 imaat neto polne` -1; • kiseli amino kiselini - jonizacijata na karboksilnata grupa osloboduve proton;
Negativno naelektrizirani amino kiselini (mono amino dikarboksilni amino kiselini)
Pozitivno naelektriziranimonokarboksilnidiamino kiselini • nivniot strani~en sinxir sodr`i pozitivni grupi; • pri rN = 7 imaat neto pozitiven polne`; • bazni amino kiselini; • strani~niot sinxir reagira so vodata, zemaj}i proton i ispu{taj}i hidroksilen anjon;
Pozitivno naelektrizirani amino kiselini (diamino monokarboksilni amino kiselini)
Podelba na amino kiselinite Spored gradbata na amino kiselinskiot ostatok Rse delat na: • alifati~ni i • cikli~ni amino kiselini - aromati~ni i - heterocikli~ni
Alifati~ni amino kiselini monamino monokarboksilni: - glicin, alanin, valin, leucin, izoleucin, serin i treonin monamino monokarboksilni {to sodr`at sulfur: - cistein, cistin i metionin. monoamino dikarboksilni i nivni amidi: - asparaginska, glutaminska, asparagin i glutamin. diamino monokarboksilni: - arginin, lizin i hidroksilizin.
Amino kiselina sostavena od 2 molekuli cistein povrzani soS-Svrska Cistin
Aromati~ni a-amino kiselini Spa|aat: - fenilalanin i tirozin
Heterocikli~ni a-amino kiselini Spa|aat: - triptofan, prolin i histidin.
PEPTIDI Soedinenija sostaveni od dve i pove}e amino kiselinski ostatoci povrzani so peptidni vrski.
PEPTIDNA VRSKA Karboksilnata grupa od edna amino kiselina se povrzuva so amino grupata od druga mino kiselina, se osloboduva voda i se sozdava amidna vrska nare~ena peptidna vrska.
PEPTIDNA VRSKA - H2O Formirawe peptidna vrska
Nomenklatura i pi{uvawe na peptidi Brojot na amino kiselinite vo malite peptidi se ozna~uvaat preku prefiksot di-, tri-, tetra- i t.n.a. od 2-10 amino kiselini - oligopeptidi od 10-100 amino kiselini- polipeptidi
Amino kiselina so slobodna a-NH3+grupa e poznata kako amino terminalna ili ednostavno N-terminalna amino kiselina Amino kiselina so slobodna -SOO- grupa e poznata kako karboksilna ili S-terminalna amino kiselina. Nomenklatura i pi{uvawe na peptidi
Struktura na pentapeptid (amino kiselinskite ostatoci se vo ramkiteGlicinot e N-terminalna, a alaninot e S-terminalna amino kiselina
Nomenklatura i pi{uvawe na peptidi Amino kiselinata koja ja vklu~uva karboksilnata grupa vo reakcija ja dobiva nastavkata -il, poslednata amino kiselina koja ja ima za~uvano -SOO- kiselinskata grupa, ostanuva so nepromeneto ime.
Nomenklatura i pi{uvawe na peptidi Ovie dva dipeptida imaat isti 2 amino kiselinski komponenti, no razli~ni amino kiselinski sekvenci
Biomedicinsko zna~ewe na peptidite Glutation • najrasprostranet priroden peptid; • tripeptid: g-glutamil-L-cisteinil-glicin; • dva mola na glutation gubat vodorod i se dobiva disulfidna forma na glutationot; • preminot na glutationot od reducirana vo oksidirana vo forma e reverzibilen oksidoredukciski proces; • va`na uloga vo organizmot vo biolo{kiot redoks potencijal.
Biomedicinsko zna~ewe na peptidite • Karnozin ili b-alanil-L-histidin, nema jasna uloga vo organizmot; • Protamini - polipeptidi so izrazen bazen karakter, povrzani so nukleinskite kiselini; • Nevropeptidite - grupa na peptidi koi se nao|aat vo centralniot nerven sistem i se pretspostavuva deka se nevrotransmiteri ili nevromodulatori, a od niv e najpoznat endorfinot. • Peptidiniteantibiotici imaat uloga da go inhibiraat rastot na mikroorganizmite, pr. penicilin. • Peptidni hormoni - od 3 do 84 amino-kiselinski ostatoci Tuka spa|aat: oksitocin, vazopresin, adenokortikotropniot hormon, melanotropinot, insulinot, kalcitoninot, paratirinot, gastrin, sekretin i dr.
PROTEINI • Imeto im poteknuva odproteus – prv • Visoko molekularni polimeri na amino kiselinite. • Mo`at da bidat sostaveni od pove}e od 100 amino kiselini • Molekulskata masa se dvi`i od 8000 do milion.
Biolo{ki funkcii Enzimi • biolo{ki katalizatori,u~estvuvaat vo mnogu metabolni reakcii Antitela • specifi~ni proteinski molekuli koi se produciraat od specijalizirani kletki od imuniot sistem; • va`ni vo odbranata na organizmot od tu|ite antigeni vklu~uvaj|i gi virusite i bakteriite; • sekoe antitelo ima region koj precizno se i povrzuva so eden antigen i pomaga vo uni{tuvawe ili otstranuvawe od teloto.
Biolo{ki funkcii Transportni proteini Gi nosat materiite od edno na drugo mesto vo teloto. Pr. transferin go transportira `elezoto od crniot drob do koskenata srcevina kade se koristi za sintezata na hem grupata na hemoglobinot. Hemoglobinot i mioglobinot se odgovorni za transport i skladirawe na kislorodot kaj vi{ite organizmi.
Biolo{ki funkcii Regulatorni proteini Gi kontroliraat od mnogu aspekti funkciite na kletkata, vklu~uvaj}i go metabolizmot i reprodukcijata Pr. hormonite: insulin i glukagon se proteini.
Biolo{ki funkcii Strukturni proteini • obezbeduvaat mehani~ka za{tita nadvore{ni oklopi; • kosata i noktite se vo najgolem del sostaveni od proteinot keratin; • drugi proteini obezbeduvaat mehani~ka za{tita na koskite, tetivite i ko`ata; • multicelularni organizmi kako nas ne bi mo`ele da egzistiraat bez niv ovie proteini.
Biolo{ki funkcii Podvi`nite proteini Potrebni za site formi na dvi`ewe. Pr. muskuli, vklu~uvaj}i gi i najva`nite muskuli, srceto, kade kontrakcijata i {ireweto odi preku interakcija na proteinite aktin i miozin. Spermatozoidite mo`e da plivaat i da oploduvaat, bidej}i tie imaat opa{ka sostavena od proteini.
Biolo{ki funkcii Hranitelni proteini Slu`at kako izvori na amino kiselini za embrionot i plodot. Albuminot od jajceto i kazeinot vo mlekoto se primeri na proteini koi se skladirani vo hranata.
STRUKTURA NA PROTEINITEPrimarna struktura • ja pretstavuva linearnata amino kiselinskata sekvenca vo proteinskiot sinxir; • rezultat od kovalentnoto povrzuvawe me|u amino kiselinite vo sinxirot (peptidini vrski), a kaj nekoi proteini i preku kovalentnite vrski na disulfidnite mostovi; • “prevod” od informacijata vo genite; • sekoj protein ima razli~na primarna struktura so razli~ni amino kiselini na razli~ni mesta dol` sinxirot;
Sekundarna struktura na proteini Pretstavuva raspored na peptidinite vrski {to ja ~inat verigata t.e. stolbot na proteinot vo prostorot. Rezultat na vodorodnite povrzuvawa me|u vodorodite od amino grupata i kislorodite od karbonil grupite od peptidnite vrski. Naj~esti se 2 tipa sekundarna struktura: - a-heliks i - b-nabrana nafaltana struktura
a-heliks Dokolku se favorizirani vodorodnite mostovi formirani vo vnatre{nosta na proteinskata molekula taa se spiralizira vo idealna desnogira a helikoidna struktura.
Va`ni karakteristiki • Sekoj amiden vodorod i karbonilen kislorod povrzani so peptidnata veriga e involviran vo gradewe vodorodnata vrska ako rastojanieto me|u grupite e 0.28 Å. • Sekoj karbonilen kislorod e vodorodno povrzan so amidniot vodorod na ~etvrtata po odale~enost amino kiselina vo sinxirot. • Vodorodnite vrski vo a-heliksot se paralelni so oskata na a-heliksot. • Rastojanieto na povtoruvawe vo a-heliksot ili negovoto jadro iznesuva 5.4 Åiima 3.6 amino kiselini vo sekoj navoj.
a-heliks a)Molekularen model na a-heliksot b)Site vodorodni vrski se paralelni so dolgata oska na heliksot. Jadroto na a-heliksot e 5.4 Åi ima 3.6 amino kiselinski ostatoci na sekoj navoj. c)Pogled od gore naa-heliksot. Strani~nite lanci od heliksot otskoknuvaat od dolgata oska na heliksot.