PHARMAKOVIGILANZ SYSTEM
PHARMAKOVIGILANZ SYSTEM. Mag. Rudolf Schranz AGES / BASG AGES Gespräch 29.11.2012. Gesetzliche Grundlagen. Volume 9b – Guidelines on Pharmacovigilance for Medicinal Products for Veterinary Use Arzneimittelgesetz. Allgemeines.

PHARMAKOVIGILANZ SYSTEM
E N D
Presentation Transcript
PHARMAKOVIGILANZSYSTEM Mag. Rudolf Schranz AGES / BASG AGES Gespräch 29.11.2012
Gesetzliche Grundlagen • Volume 9b – Guidelines on PharmacovigilanceforMedicinal Products forVeterinaryUse • Arzneimittelgesetz
Allgemeines • Teil des Dossiers (Part 1) jede Änderung ist eine Variation • Gibt Überblick über PV Aktivitäten • Wenn produktspezifische Zusätze Produktspezifisches Addendum
Inhalt Statement des Zulassungsinhabers und der QPPV bezüglich der Verfügbarkeit und Möglichkeiten der Meldung von Nebenwirkungen • Von MAH und QPPV zu unterschreiben • Kann Verweis auf DDPS enthalten
Inhalt QualifiedPerson ResponsibleforPharmacovigilance • Sitz im EWR • Kontaktdaten (Name, Adresse, Telefon) • 24 Stunden Erreichbarkeit • CV (Qualifikation, Ausbildung, Expertise) • Job description • Beschreibung der Backup Procedure
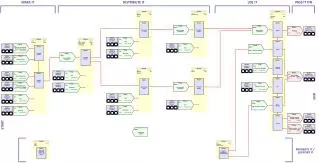
Inhalt Angaben zur Organisation • Name und Adresse der EU und globalen PV Aktivitäten (Ort der Datenbanken), Angabe wo die PV Daten verfügbar sind • Organigramm • Kurzzusammenfassung der PV Aktivitäten der im Organigramm angeführten Stellen • Flußdiagrammüber Lauf einer Meldung
Inhalt Prozesse und SOP´s • Welche Prozesse werden durch welche SOP´s abgedeckt • SOP´s nicht dem DDPS beilegen jede Änderung wäre dann Variation • Liste und SOP´s müssen in zwei Werktagen nach Behördenanforderung verfügbar sein
Inhalt Wesentliche Prozesse • QPPV: Aktivitäten und Backup Procedure • NW Meldungen: Eingang, Vorgang bei fehlenden Inhalten, Dateneingabe und –mamagement, Kodierung, Klassifikation, Veterinärreview, Reporting • Sicherstellen, dass Berichte aus verschiedenen Quellen abgedeckt sind:
Inhalt • EWR und Drittlandmeldungen, Tierärzte, andere HCP, Tierbesitzer • Sales und Marketing • Andere MAH und Behörden
Inhalt • Duplikatdetektion • Expeditedreporting • Elektronische Meldung (EudraVigilance) • PSUR´s
Inhalt - Datenbanken Datenbanken • Verwendete Datenbanksysteme • Kurze Funktionsbeschreibung • Verantwortlichkeiten für Funtion • Standort • Statement zum Validierungsstatus • Compliance mit internationalen Standard für elektronische Meldungen (entspr. PART III) • Kopie der Registrierung der QPPV bei EudraVigilance
Inhalt - Verträge Verträge • PV relevant • Vereinbarungen zu Co-Lizenzierungen Co-Marketing • Im EWR • Verantwortlichkeiten der beteiligten Partner • Falls Produktspezifisch Produktspezifisches Addendum • Kurzbeschreibung der Verträge mit • Co-Marketing Partner • Partner in Pharmakovigilanzagenden
Inhalt - Training Angaben zum Training • Für alle Mitarbeiter über die potentiell Meldungen eingehen können (Sales, Monitore, Marketing …) • Nicht nur Pharmakovigilanz Personal • Kurzbeschreibung des Trainingsystems • Ort wo Trainingsbestätigungen, CV und Job descriptions archiviert werden
Inhalt - Dokumentation • Kurzbeschreibung wo die Source Daten der Meldungen aus den verschiedenen Quellen abgelegt werden • Bezug auf das „Organisational chart“ ist möglich • Informationen über Archivvereinbarungen
Inhalt - Qualitätsmanagement • Kurzbeschreibung des Qualitätsmanagementsystems • Referenzierungen auf andere Inhalte des PV Systems sind möglich • Kurzbeschreibung des Auditsystems des PV Systems inklusive Audits bei Partner • Schwerpunkte sollen Organisatorische Rollen und Verantwortlichkeiten für Aktivitäten und Dokumentation • Qualitätskontrollen • Review • Sicherstellung von correctiveactions und Vorbeugemaßnahmen
Inhalt • Der Zulassungsinhaber muß sicherstellen, dass das PV System etabliert und dokumentiert ist • Die Funktionen und Verantwortlichkeiten müssen den beteiligten Personen und Partner bekannt sein • Das PV System muss entsprechend kontrolliert und bei Bedarf geändert werden
Kontakt Mag. Brigitte Hauser allgemeine E-Mail: brigitte.hauser@ages.atpharm-vigilanz@ages.at +43 (0) 50555 36257 Mag. Rudolf Schranz fax: rudolf.schranz@ages.at +43 (0) 50555 36207 +43 (0) 50555 36246 Brigitte Hauser
links www.basg.gv.at www.ages.at www.ema.europa.eu www.hma.eu www.vichsec.org Brigitte Hauser